题目内容
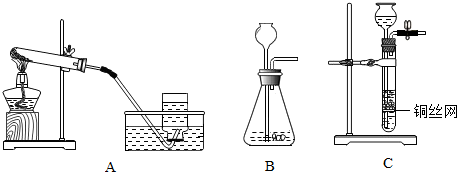
20、通过化学学习,你已经掌握了实验室制取气体的一般规律,下列为实验室常用的实验装置,回答问题:
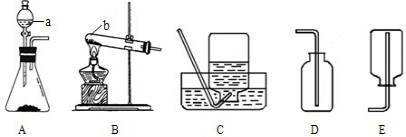
(1)写出图中标号的仪器名称:a
(2)实验室用高锰酸钾制取氧气时应选用
(3)实验室常用稀盐酸和石灰石反应制CO2,应选用的发生装置是
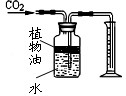
(4)右图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是

(1)写出图中标号的仪器名称:a
分液漏斗
,b试管
;(2)实验室用高锰酸钾制取氧气时应选用
B
(填字母标号,下同)做气体发生装置;如果用D装置收集氧气,那么检验氧气是否收集满的方法是用带火星的木条平放在集气瓶口,如带火星的木条复燃,则氧气已满
.(3)实验室常用稀盐酸和石灰石反应制CO2,应选用的发生装置是
A
,收集装置是D
.写出该反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O
;此外,也可用加热碳酸氢钠(NaHCO3)固体来制取CO2,则应选用的发生装置为B
.(4)右图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是
使CO2气体与水隔离,防止二氧化碳溶解于水
,植物油上方原有的空气对实验结果无
(填“有”或“无”)明显影响.
分析:(1)根据仪器的形状、结构、用途等回答.
(2)根据实验室用高锰酸钾制取氧气时药品的状态、反应的条件,以及氧气的助燃性回答.
(3)根据实验室制二氧化碳的原理、药品的状态和反应条件,以及碳酸氢钠的状态、及其生成二氧化碳的反应条件回答.
(4)根据二氧化碳的溶解性及量气装置量气体体积的原理回答.
(2)根据实验室用高锰酸钾制取氧气时药品的状态、反应的条件,以及氧气的助燃性回答.
(3)根据实验室制二氧化碳的原理、药品的状态和反应条件,以及碳酸氢钠的状态、及其生成二氧化碳的反应条件回答.
(4)根据二氧化碳的溶解性及量气装置量气体体积的原理回答.
解答:解:(1)a是加入液体药品的仪器,有盖和活塞,是分液漏斗;b是少量试剂的反应容器,是试管.
(2)实验室用高锰酸钾制取氧气所用药品为固体,反应条件是加热,发生装置应选B;如果用向上排空气法收集氧气,验满时的操作方法为:用带火星的木条平放在集气瓶口,如带火星的木条复燃,则氧气已满.
(3)实验室制二氧化碳所用药品是固态的石灰石与液态的稀盐酸,反应不需加热,气体发生装置选用A,二氧化碳能溶于水不能用排水法收集,因密度比空气大,可用向上排空气法,装置选用D;反应原理是碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;如用加热碳酸氢钠(NaHCO3)固体来制取CO2,药品状态为固体,条件为加热,发生装置要选用B.
(4)二氧化碳能溶于水,但不能溶解于植物油,为了防止二氧化碳溶解于水中,在水面上放一层植物油;量所装置是通过二氧化碳排出水的体积来确定二氧化碳的体积,开始时植物油上方原有的空气没有与外界形成气压差,故对实验结果无影响.
故答案为:(1)a、分液漏斗;b、试管;(2)B;用带火星的木条平放在集气瓶口,如带火星的木条复燃,则氧气已满;(3)A;D;CaCO3+2HCl=CaCl2+CO2↑+H2O;B;(4)使CO2气体与水隔离,防止CO2溶于水;无.
(2)实验室用高锰酸钾制取氧气所用药品为固体,反应条件是加热,发生装置应选B;如果用向上排空气法收集氧气,验满时的操作方法为:用带火星的木条平放在集气瓶口,如带火星的木条复燃,则氧气已满.
(3)实验室制二氧化碳所用药品是固态的石灰石与液态的稀盐酸,反应不需加热,气体发生装置选用A,二氧化碳能溶于水不能用排水法收集,因密度比空气大,可用向上排空气法,装置选用D;反应原理是碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;如用加热碳酸氢钠(NaHCO3)固体来制取CO2,药品状态为固体,条件为加热,发生装置要选用B.
(4)二氧化碳能溶于水,但不能溶解于植物油,为了防止二氧化碳溶解于水中,在水面上放一层植物油;量所装置是通过二氧化碳排出水的体积来确定二氧化碳的体积,开始时植物油上方原有的空气没有与外界形成气压差,故对实验结果无影响.
故答案为:(1)a、分液漏斗;b、试管;(2)B;用带火星的木条平放在集气瓶口,如带火星的木条复燃,则氧气已满;(3)A;D;CaCO3+2HCl=CaCl2+CO2↑+H2O;B;(4)使CO2气体与水隔离,防止CO2溶于水;无.
点评:气体的制取是初中重要的化学实验之一,既是难重点,又是考查热点,理解反应原理,掌握装置的选择依据、气体的检验、验满、收集方法,了解实验步骤和注意事项是解决该类问题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
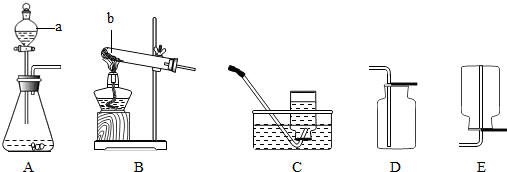
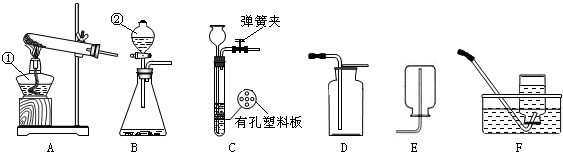
 通过化学学习,你已经掌握了实验室制取气体的一些规律,请结合下图回答问题:
通过化学学习,你已经掌握了实验室制取气体的一些规律,请结合下图回答问题: