题目内容
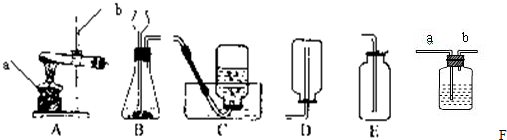
实验室常用下列装置来制取氧气:

(1)写出图中有标号仪器的名称:a
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是
应
(3)检验氧气是否集满的方法是
(4)化学兴趣小组在实验室用过氧化氢溶液和二氧化锰粉末制取氧气,但对老师提供的一瓶标签模糊的“■■水”产生了争议,小明认为是蒸馏水,小华认为是俗称“双氧水”的过氧化氢溶液.请你帮助他们检验该瓶试剂.
(5)小华同学从资料上看到“红砖粉可作为过氧化氢溶液分解反应中的催化剂”,就这一命题,她设计并完成了下表所示的探究实验:
①在小华的探究实验中,实验一和实验二起的作用是
②小明同学认为仅由上述实验还不能完全得出表内“总结”,他补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:

(1)写出图中有标号仪器的名称:a
酒精灯
酒精灯
、b铁架台
铁架台
;(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是
B
B
(填序号),收集好的氧气应
正放
正放
(“正放”或“倒放”)实验台上,写出该反应的符号表达式2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
| ||
(3)检验氧气是否集满的方法是
将带火星的木条放于集气瓶口,若木条复燃,说明收集满了
将带火星的木条放于集气瓶口,若木条复燃,说明收集满了
.(4)化学兴趣小组在实验室用过氧化氢溶液和二氧化锰粉末制取氧气,但对老师提供的一瓶标签模糊的“■■水”产生了争议,小明认为是蒸馏水,小华认为是俗称“双氧水”的过氧化氢溶液.请你帮助他们检验该瓶试剂.
| 操作步骤 | 现象 | 结论 |
取少量的液体于试管中,向其中加入少量二氧化锰 取少量的液体于试管中,向其中加入少量二氧化锰 |
若反应产生气泡 若无现象 若反应产生气泡 若无现象 |
该液体为双氧水 该液体为蒸馏水 该液体为双氧水 该液体为蒸馏水 |
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 各步骤结论 | 总结 | |||
| 实验一 | 在一支试管中倒入一定量的过氧化氢溶液,伸入带火星的木条, | 有极少量的细小气泡,木条不复燃 | 过氧化氢溶液常温下能产生极少量的氧气 | 红砖粉是过氧化氢分解的催化剂 |
| 实验二 | 加入少量红砖粉,伸入带火星的木条, | 木条复燃 | 过氧化氢溶液和红砖粉混合能迅速产生氧气. | |
对比(或对照等)
对比(或对照等)
;②小明同学认为仅由上述实验还不能完全得出表内“总结”,他补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:
比较红砖粉在过氧化氢分解前后质量是否发生变化
比较红砖粉在过氧化氢分解前后质量是否发生变化
;第二方面的实验是需要证明红砖粉的化学性质是否改变
红砖粉的化学性质是否改变
.分析:(1)据常用仪器回答;
(2)据过氧化氢制取氧气的反应物状态和反应条件选择发生装置,氧气密度比空气大,故应正放在桌面上,据反应原理书写符号表达式;
(3)检验氧气是否集满的方法是:将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(4)根据过氧化氢的性质设计实验进行判断,常温下双氧水在二氧化锰催化下可分解放出氧气,而蒸馏水常温下不能分解;
(5)在验证红砖粉的催化作用时,可设计对比实验,利用对比实验说明红砖粉能加快反应的速度,且反应前后二氧化锰的质量的化学性质保持不变.
(2)据过氧化氢制取氧气的反应物状态和反应条件选择发生装置,氧气密度比空气大,故应正放在桌面上,据反应原理书写符号表达式;
(3)检验氧气是否集满的方法是:将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(4)根据过氧化氢的性质设计实验进行判断,常温下双氧水在二氧化锰催化下可分解放出氧气,而蒸馏水常温下不能分解;
(5)在验证红砖粉的催化作用时,可设计对比实验,利用对比实验说明红砖粉能加快反应的速度,且反应前后二氧化锰的质量的化学性质保持不变.
解答:解:(1)标号仪器分别是酒精灯、铁架台;
(2)用双氧水和二氧化锰来制取氧气时,不需加热,属于固液常温型,故选发生装置B,氧气密度比空气大,故应正放在桌面上,反应的符号表达式是:2H2O2
2H2O+O2↑;
(3)检验氧气是否集满的方法是:将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(4)可取适量无色液体加入少量二氧化锰,若有气体产生,则可说明无色液体为双氧水即过氧化氢溶液;
(5)①红砖粉只是改变化学反应的速率,所以在设计实验时设计了两个对比实验:一个实验在试管中只放双氧水,双氧水也能分解产生氧气,但产生氧气的速度太慢.第二个实验,在试管中既放双氧水也放红砖粉,能很快的放出氧气;
②为了说明红砖粉在此实验中反应前后的质量保持不变.做了两次称量,目的是比较红砖粉反应前后质量是否变化.还需要验证红砖粉在反应后的化学性质是否改变;
故答案为:
(1)酒精灯;铁架台;
(2)B;正放;2H2O2
2H2O+O2↑;
(3)将带火星的木条放于集气瓶口,若木条复燃,说明收集满了;
(4)
(5)①对比(或对照等);②比较红砖粉在过氧化氢分解前后质量是否发生变化;红砖粉的化学性质是否改变.
(2)用双氧水和二氧化锰来制取氧气时,不需加热,属于固液常温型,故选发生装置B,氧气密度比空气大,故应正放在桌面上,反应的符号表达式是:2H2O2
| ||
(3)检验氧气是否集满的方法是:将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(4)可取适量无色液体加入少量二氧化锰,若有气体产生,则可说明无色液体为双氧水即过氧化氢溶液;
(5)①红砖粉只是改变化学反应的速率,所以在设计实验时设计了两个对比实验:一个实验在试管中只放双氧水,双氧水也能分解产生氧气,但产生氧气的速度太慢.第二个实验,在试管中既放双氧水也放红砖粉,能很快的放出氧气;
②为了说明红砖粉在此实验中反应前后的质量保持不变.做了两次称量,目的是比较红砖粉反应前后质量是否变化.还需要验证红砖粉在反应后的化学性质是否改变;
故答案为:
(1)酒精灯;铁架台;
(2)B;正放;2H2O2
| ||
(3)将带火星的木条放于集气瓶口,若木条复燃,说明收集满了;
(4)
| 作步骤 | 现象 | 结论 |
| 取少量的液体于试管中,向其中加入少量二氧化锰 | 若反应产生气泡 若无现象 |
该液体为双氧水 该液体为蒸馏水 |
点评:本题考查知识较为全面,尤其是对过氧化氢制取氧气的相关知识的考查,在确定一种物质是催化剂时,不但要确定它能否改变化学反应的速率,还要确定它反应前后的质量和化学性质是否改变.只有这两条都不变,才是催化剂.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目


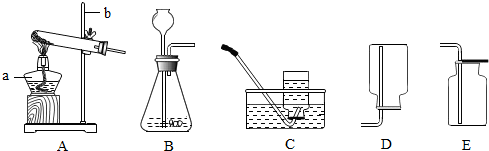
 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气: