题目内容
(2012?顺义区二模)铁及其化合物在生产生活中应用广泛.
(1)铁矿石是工业炼铁的主要原料之一.下列铁矿石中属于氧化物的是

其中以磁铁矿石为原料炼铁的化学方程式为
(2)铁红是红色的颜料,其成分是Fe2O3.将一定量的铁红放入适量稀盐酸中,反应的化学方程式为
(3)氯化铁溶液常用作印刷电路板的腐蚀剂,其过程发生如下2FeCl3+Cu=2FeCl2+CuCl2.取反应所得氯化亚铁和氯化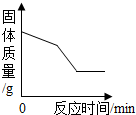 铜的混合溶液,加入一定量的锌粉,有如图所示的反应关系.则下列说法正确的是
铜的混合溶液,加入一定量的锌粉,有如图所示的反应关系.则下列说法正确的是
A.向反应后的固体中滴加稀盐酸,一定有气泡产生
B.反应后的溶液中一定没有氯化亚铁
C.反应后的溶液中一定没有氯化铜
D.反应后的固体中一定含有Cu、Fe、Zn.
(1)铁矿石是工业炼铁的主要原料之一.下列铁矿石中属于氧化物的是
AD
AD
(填字母).
其中以磁铁矿石为原料炼铁的化学方程式为
4CO+Fe3O4
4CO2+3Fe
| ||
4CO+Fe3O4
4CO2+3Fe
.
| ||
(2)铁红是红色的颜料,其成分是Fe2O3.将一定量的铁红放入适量稀盐酸中,反应的化学方程式为
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
.向反应后的溶液中加入一定量铁粉,铁粉消失,溶液变为浅绿色,反应的化学方程式为2FeCl3+Fe=3FeCl2
2FeCl3+Fe=3FeCl2
.(3)氯化铁溶液常用作印刷电路板的腐蚀剂,其过程发生如下2FeCl3+Cu=2FeCl2+CuCl2.取反应所得氯化亚铁和氯化
 铜的混合溶液,加入一定量的锌粉,有如图所示的反应关系.则下列说法正确的是
铜的混合溶液,加入一定量的锌粉,有如图所示的反应关系.则下列说法正确的是AC
AC
(填字母).A.向反应后的固体中滴加稀盐酸,一定有气泡产生
B.反应后的溶液中一定没有氯化亚铁
C.反应后的溶液中一定没有氯化铜
D.反应后的固体中一定含有Cu、Fe、Zn.
分析:(1)根据氧化物的特点和方程式的书写考虑;(2)根据方程式的书写方法考虑;(3)根据图示可知锌先与氯化铜反应,再与氯化亚铁反应,根据图示考虑反应情况,再进行分析.
解答:解:(1)氧化物是由两种元素组成,一种是氧元素,所以AD属于氧化物;反应物是一氧化碳和四氧化三铁,生成物是铁和二氧化碳,用观察法配平,反应条件是高温写在等号的上边;
(2)铁红放入适量稀盐酸中反应物是氧化铁和盐酸,生成物是氯化铁和水,用观察法配平;溶液中加入一定量铁粉,铁粉消失,溶液变为浅绿色,浅绿色是亚铁离子的颜色,所以反应物是铁和氯化铁,生成物是氯化亚铁,用最小公倍数法配平;
(3)根据图示可知锌先与氯化铜反应,再与氯化亚铁反应,并且已经把氯化铜完全反应完了,与氯化亚铁的反应有两种可能:可能反应完了,可能没反应完,锌与氯化亚铁反应生成铁和氯化锌,所以反应后的固体中一定含有铁,所以加入盐酸一定能产生氢气,所以A说法正确;锌与氯化亚铁的反应有两种可能:可能反应完了,可能没反应完,所以反应后的溶液中可能含有氯化亚铁;由于已经把氯化铜完全反应完了,所以反应后的溶液中一定没有氯化铜;反应后的固体中一定含有Cu、Fe,可能含有锌.
故答案为:(1)AD;4CO+Fe3O4
4CO2+3Fe;(2)Fe2O3+6HCl=2FeCl3+3H2O;2FeCl3+Fe=3FeCl2;(3)AC.
(2)铁红放入适量稀盐酸中反应物是氧化铁和盐酸,生成物是氯化铁和水,用观察法配平;溶液中加入一定量铁粉,铁粉消失,溶液变为浅绿色,浅绿色是亚铁离子的颜色,所以反应物是铁和氯化铁,生成物是氯化亚铁,用最小公倍数法配平;
(3)根据图示可知锌先与氯化铜反应,再与氯化亚铁反应,并且已经把氯化铜完全反应完了,与氯化亚铁的反应有两种可能:可能反应完了,可能没反应完,锌与氯化亚铁反应生成铁和氯化锌,所以反应后的固体中一定含有铁,所以加入盐酸一定能产生氢气,所以A说法正确;锌与氯化亚铁的反应有两种可能:可能反应完了,可能没反应完,所以反应后的溶液中可能含有氯化亚铁;由于已经把氯化铜完全反应完了,所以反应后的溶液中一定没有氯化铜;反应后的固体中一定含有Cu、Fe,可能含有锌.
故答案为:(1)AD;4CO+Fe3O4
| ||
点评:本题容易出错的地方是第(3)小题,要通过图示看出锌先与氯化铜反应,又和氯化亚铁反应,且锌与氯化铜已经反应完了,再进行具体分析.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目