题目内容
【题目】大气污染会破坏生态系统,我国在防治大气污染方面做了大量工作。一氧化碳是大气污染物之一。
(1)通过燃烧反应,CO可转化成无污染的CO2。2个CO分子完全反应,可生成CO2分子_____个。
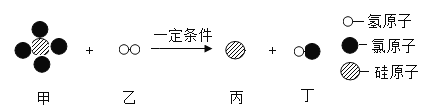
(2)汽车尾气的催化转化装置可有效降低CO和氮氧化物(如NO)的排放,减少空气污染。催化转化过程可分为储存和还原两个步骤,反应原理如下图所示:
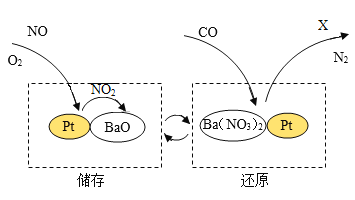
①通过储存和还原,BaO可实现循环利用,是尾气处理过程中的催化剂。某汽车尾气净化装置中装入BaO的质量为0.5kg,使用一年后其质量为_____0.5kg(填“>”“=”“<”)。
②还原时,发生反应的化学方程式为:![]() ,推测X的化学式是_____。
,推测X的化学式是_____。
【答案】2 = BaO
【解析】
(1)一氧化碳在氧气中燃烧生成二氧化碳,反应的化学方程式为:2CO+O2![]() 2CO2;根据化学方程式可知,2个CO分子完全反应,可生成CO2分子2个;
2CO2;根据化学方程式可知,2个CO分子完全反应,可生成CO2分子2个;
(2)①催化剂在化学反应前后质量不变。通过储存和还原,BaO可实现循环利用,是尾气处理过程中的催化剂。某汽车尾气净化装置中装入BaO的质量为0.5kg,使用一年后其质量为=0.5kg;
②根据还原时,发生反应的化学方程式:![]() 可知,反应前的碳原子、氧原子、钡原子、氮原子分别为5、11、1、2,反应后的碳原子、氧原子、钡原子、氮原子分别为5、10、0、2,根据化学反应中原子的种类和数目不变,推测X的化学式是BaO。
可知,反应前的碳原子、氧原子、钡原子、氮原子分别为5、11、1、2,反应后的碳原子、氧原子、钡原子、氮原子分别为5、10、0、2,根据化学反应中原子的种类和数目不变,推测X的化学式是BaO。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
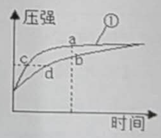
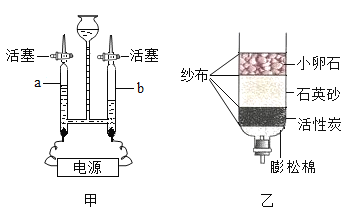
暑假衔接培优教材浙江工商大学出版社系列答案【题目】纯水的导电能力很弱,电解水时常在水中加入一些NaOH增强导电性。为研究影响电解水反应速率的因素,某课外活动小组进行了实验探究,数据记录如下表(直流电,电压: 12V):
实验编号 | 温度(°C) | NaOH溶液浓度(%) | H2体积(mL) | O2体积( mL) | 电解时间(s) |
a | 20 | 2% | 20 | 9.8 | 54.0 |
b | 20 | 5% | 20 | 9.8 | 36.2 |
c | 30 | 2% | 20 | 9.6 | 46.2 |
d | 30 | 5% | 20 | 9.7 | X |
请回答问题:
(1)电解水反应的化学方程式为_____。
(2)该小组研究的影响电解水反应速率的因素是_____和_____。
(3)本实验通过比较_____确定电解水速率的快慢。
(4)比较实验a和c,可得到的结论是:_____。
(5)分析实验a、b、c的数据,实验d的电解时间“X”是_____。
A 35.4
B 37.8
C 50.2
D 55.6
(6)理论上,电解水产生H2、O2 的体积比为2:1,但实验结果比大于理论值,请从两种气体物理性质分析,可能的原因是_____。
【题目】人们的生产、生活与化学密不可分。
(1)可用来生产触摸屏的主要原料是氧化铟(In2O3),氧化铟中铟(In)的化合价为_____。
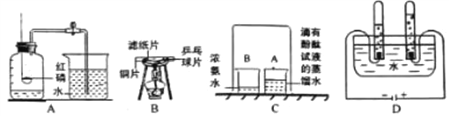
(2)防雾霾口罩透气空隙小,可以把直径较大的颗粒物阻挡在外,其原理与_____(填化学操作名称)类似。
(3)“自热火锅”主要由料包和发热包(主要成分为生石灰、焙烧硅藻土、活性炭等)组成,发热包发热的一种原理是生石灰与水反应。化学方程式可表示为_____。烧硅藻土、活性炭都有_____的结构,能起到吸附作用。
(4)下表是我国颁布的生活饮用水水质标准的部分内容。
项目 | 标 准 |
感官指标 | 无异味、异臭等 |
化学指标 | 铜<1.0mgL,铁<0.3mgL,氟化物<1.0mgL,游离氯≥0.3mgL等 |
感官指标表现的是自来水的_____(填“物理性质”或“化学性质”);化学指标中的铜、铁是指_____(填“元素”或“单质”)。自来水中因含有较多的Ca2+和镁离子_____(填离子符号)被称为硬水。