题目内容
【题目】达州盛产天然气,有“中国气都”之称的美誉.天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,参与探究。
【提出问题】:甲烷燃烧后生成哪些物质?
【查阅资料】:含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】:
猜想甲: CO2 H2O;
猜想乙: CO2 CO H2O;
猜想丙: ______________
【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过如图所示装置:
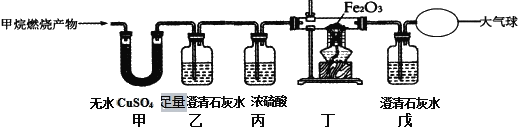
(1)甲、乙装置的顺序能否颠倒?_______(填“能“或“否”)
(2)实验中用纯净O2而不用空气的原因是 _____________________ 。
(3)实验中观察到甲中无水CuSO4变蓝,乙、戊中澄清石灰水变浑浊,丁中红色粉末变成黑色,由此推断_______ 同学猜想成立。
(4)装置乙的作用是___________________________,写出丁中发生的化学反应化学方程式:________________________ 。
【反思与交流】:为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是__________________________。
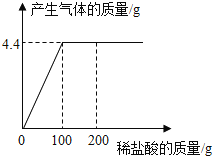
实验结束,对相关装置进行称量(忽略空气成分对实验的干扰):甲装置增重3.6g,乙装置增重2.2g。那么燃烧甲烷的质量为 _____ g,并写出该实验中甲烷燃烧的化学方程式 __________________________________________。
【答案】 CO和H2O 否 空气中CO2和水蒸气影响实验测定 乙 检验并除去CO2 3CO+F2O3![]() 2Fe+3CO2 提供充足氧气 1.6 4CH4+7O2
2Fe+3CO2 提供充足氧气 1.6 4CH4+7O2![]() 2CO2+2CO+8H2O
2CO2+2CO+8H2O
【解析】【猜想与假设】根据质量守恒定律可知化学反应前后元素的种类不变,反应物中是甲烷和氧气,如果不完全燃烧生成一氧化碳和水;
(1)如果顺序颠倒,由于石灰水中有水,就不能证明混合气体中是否有水;
(2)由于空气中含有水分和二氧化碳,用空气就无法验证混合气体中是否含有水和二氧化碳,因为到底是混合气体中的水和二氧化碳,还是空气中的水和二氧化碳,无法确定;
(3)甲中无水CuSO4变蓝说明混合气体中有水,乙中石灰水变浑浊说明混合气体中含有二氧化碳,乙中石灰水有两个作用:验证二氧化碳的存在,除去二氧化碳;戊中澄清石灰水变浑浊,丁中红色粉末变成黑色说明具有还原性气体,且与氧化铁反应能生成二氧化碳,所以说明混合气体中含有一氧化碳;
(4)乙中石灰水有两个作用:验证二氧化碳的存在,除去二氧化碳;丁中红色粉末变成黑色的反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,用得失氧进行配平,反应条件是高温,写在等号的上边,化学方程式为:3CO+F2O3![]() 2Fe+3CO2。
2Fe+3CO2。
【反思与交流】由于可燃物不完全燃烧能生成一氧化碳,污染环境,所以要让可燃物完全燃烧,所以需要充足的氧气;
如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中的水;
3.6g水中氢元素的质量为:3.6g×![]() ×100%=0.4g,
×100%=0.4g,
甲烷中氢元素的质量完全转化到水中,因此甲烷的质量为:0.4g÷(![]() ×100%)=1.6g,
×100%)=1.6g,
甲烷中碳元素的质量为:1.6g-0.4g=1.2g,
2.2g二氧化碳中碳元素的质量为:2.2g×![]() ×100%=0.6g,
×100%=0.6g,
甲烷燃烧同时生成了一氧化碳,一氧化碳中碳元素的质量为:1.2g-0.6g=0.6g,
则生成的一氧化碳质量为:0.6g÷(![]() ×100%)=1.4g,
×100%)=1.4g,
则反应的氧气质量为:3.6g+2.2g+1.4g-1.6g=5.6g,
反应物甲烷、氧气和生成物二氧化碳、一氧化碳、水的分子个数比为: ![]() =4:7:2:2:8,
=4:7:2:2:8,
甲烷燃烧的化学方程式为:4CH4+7O2![]() 2CO2+2CO+8H2O。
2CO2+2CO+8H2O。

 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】在实验室中甲乙两位同学分别进行了如下实验,其中甲观察到固体全部消失有气泡冒出,甲同学实验中发生的反应类型是______,乙同学实验中观察到的现象是______。反应结束后甲乙两位同学将仪器中药品全部倒在一个大烧杯中后观察到有气泡冒出和大量白色沉淀生成。

【问题】:反应后大烧杯中上层清液中中含有哪些溶质?
【猜想】:①可能只含有:NaCl ②可能含有CaCl2、NaCl ③可能含有CaCl2、NaCl 和 Na2CO3 ④ 可能含有、NaCl 、Na2CO3 。
甲乙两位同学通过讨论一致认为上述猜想_____ 一定不成立,理由是_________。
【实验】:
实验步骤 | 实验现象 | 实验结论 |
1、取少量上层清液于一支试管中,滴加足量K2CO3溶液 | ___________ | 猜想②不成立 |
2、取少量上层清液于一支试管中,滴加足量Ba(NO3)2溶液 | 白色沉淀 | 猜想________ 成立 |
3、取少量上层清液于一支试管中,滴加1-2滴酚酞 | ___________ |