题目内容
(2010?西城区二模)汽车尾气排放出的主要气体有NO和NO2,它们污染环境.可用氨气(NH3)除去有害气体,该反应的化学方程式为:2NH3+NO+NO2 2N2+3H2O.若反应后得到2.8gN2,理论上需要氨气的质量多少克?
2N2+3H2O.若反应后得到2.8gN2,理论上需要氨气的质量多少克?
【答案】分析:根据化学方程式,得出各物质之间的质量比,列出比例式,即可计算出需要氨气的质量.
解答:解:设需要氨气的质量为x,
2NH3+NO+NO2 2N2+3H2O
2N2+3H2O
34 56
x 2.8g
∴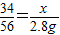
解之得:x=1.7g,
答:理论上需要氨气的质量为1.7g.
点评:本题主要考查学生运用化学方程式进行计算的能力.
解答:解:设需要氨气的质量为x,
2NH3+NO+NO2
 2N2+3H2O
2N2+3H2O34 56
x 2.8g
∴
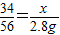
解之得:x=1.7g,
答:理论上需要氨气的质量为1.7g.
点评:本题主要考查学生运用化学方程式进行计算的能力.

练习册系列答案
相关题目

