题目内容
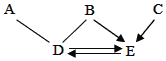
【题目】A、B、C、D、E是初中阶段常见物质,A、B、D、E分别是四种不同物质类别的化合物,E是导致温室效应的气体。它们存在如图所示的转化关系,“→”表示可以向箭头所指方向一步转化,“﹣”表示两种物质之间可以发生反应。请回答下列问题:
(1)A物质的类别:_____。(选填“氧化物”、“酸”、“碱”、“盐”)
(2)写出A和D反应的化学方程式:_____。
(3)写了C→E的化学方程式:_____,该反应基本类型是_____。
【答案】碱 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH C+O2![]() CO2 化合反应
CO2 化合反应
【解析】
A、B、C、D、E是初中阶段常见物质,E是导致温室效应的气体。则E是二氧化碳,D和二氧化碳能相互转化,则D可能是碳酸盐,结合盐的性质,D可以和A、B反应,A、B、D、E分别是四种不同物质类别的化合物,则A和B是酸或碱,又因为B能得到二氧化碳,因此,A是碱,B是酸,C能得到二氧化碳,C可以是木炭,A可以是氢氧化钙。B可以是稀盐酸,D可以是碳酸钠。将猜想代入关系图,猜想成立。
根据以上分析可知:
(1)A物质的类别是碱类;
(2)A和D反应的化学方程式可以是氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)C→E的反应可以是木炭燃烧生成二氧化碳,化学方程式:![]() ;反应物是两种,生成物是一种,属于化合反应。
;反应物是两种,生成物是一种,属于化合反应。

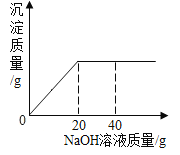
【题目】某同学对若干块矿石样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应).请计算:
序号 | 加入稀盐酸质量(g) | 剩余固体质量(g) |
第1次 | 10 | 5.5 |
第2次 | 10 | m |
第3次 | 10 | 1.2 |
第4次 | 10 | 1.2 |
(1)8g的石灰石样品中含有杂质 克?
(2)如表中m的数值应为 ?
(3)稀盐酸的质量分数是多少?
【题目】自来水消毒过程中常发生下列转化:
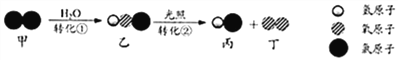
下列说法正确的是 ( )
A. 反应前后分子不可分 B. 转化①是化合反应
C. 转化②中丙和丁的分子个数之比为1︰1 D. 转化①、②中氯元素的化合价都发生变化
【题目】干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质。某研究 小组对一只干燥管里的碱石灰样品的成分进行实验探究。
(提出猜想) 猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠; 猜想Ⅱ:已经变质,可能情况未知;猜想Ⅲ:完全变质,且只含有碳酸钙和碳酸钠;
(实验探究)
(1)取样品,加入几滴清水,试管外壁不发烫;
(2)取样品,加入足量清水和几滴酚酞溶液,充分搅拌并过滤,得到白色沉淀和红色滤液;
(分析过程)
根据实验(1)说明猜想_____(填“Ⅰ”、“Ⅱ”或“Ⅲ”)不成立。根据实 验(2)甲同学认为猜想Ⅲ成立,乙同学不同意,他认为碱石灰样品中不一定含有碳酸钙, 可能含有氢氧化钙,他的理由是_________(请写化学方程式)。
为进一步确定猜想,他们设计了以下实验方案:
实验方案 | 实验现象 | 分析 |
①取红色滤液,通入一定_____ 量的 CO2 气体 | 若产生_______ | 滤液中含有 Ca(OH)2 |
②取红色滤液,加入过量 的_____溶液 | 若产生白色沉淀,溶液仍然呈红色 | 滤液中含有_______ |
若产生白色沉淀,溶液呈无色 | 滤液中只含 Na2CO3 |
(实验结论)甲、乙同学完成设计的实验方案后,证明了猜想Ⅱ成立。
(实验反思)根据上述实验,下列说法正确的是_____(填序号)。
A 过滤后得到的红色滤液中的溶质只有 3 种可能的组合
B 表格中的方案①,若通入的 CO2 适量,溶液可能由红色变成无色
C 实验证明了原碱石灰样品中一定不含 CaCO3
D 根据实验可知,碱石灰样品的变质情况有 2 种可能性