题目内容
【题目】(1)计算硝酸铵(NO3NH4)中氮元素的质量分数;
(2)计算尿素(CO(NH2)2)中氮元素的质量分数;
(3)假设市场销售的硝酸铵和尿素每袋的质量都是50千克,每袋硝酸铵的售价是50元,每袋尿素的售价是80元,某人现在有现金400元准备给庄稼追氮肥,请同学们为他设计一下,买那种化肥最合算?
【答案】35% ;46.7% ;买硝酸铵合算
【解析】
首先利用化学式计算出两种化肥中氮元素的质量分数,再计算出400元所买两种化肥中氮元素的质量,氮元素质量多的就合算。
(1)解:硝酸铵中氮元素的质量分数=![]() ×100%=35%
×100%=35%
答:硝酸铵中氮元素的质量分数为35%。
(2)解:尿素中氮元素的质量分数=![]() 100%=46.7%
100%=46.7%
答:尿素中氮元素的质量分数为46.7%。
(3)解:所买硝酸铵中氮元素的质量=50千克×![]() 35%=140千克;
35%=140千克;
所买尿素中氮元素的质量=50千克×![]() ×46.7%=116.75千克
×46.7%=116.75千克
140千克>116.75千克
答:买硝酸铵比较合算。

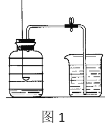
【题目】某课外小组的同学将玻璃罩内充满纯净的二氧化碳气体,如图A所示,在光照充足的条件下,经过一段时间后,该小组同学用注射器从a处抽取气体,测定玻璃罩内气体的成分及其含量。

(查阅资料)
①植物通过光合作用吸收二氧化碳气体,放出氧气。
②氢氧化钠(NaOH)和氢氧化钙性质相似,其水溶液也能和二氧化碳发生反应,且没有沉淀和气体物质生成。
(实验一)检验玻璃罩内是否含有二氧化碳气体?
实验步骤 | 实验现象 | 实验结论 |
抽取适量气体,注入________中 | ____________ | 玻璃罩内含有二氧化碳 |
将上述表格中的实验步骤和现象补充完整。
(实验二)采用两种方法测定玻璃罩内气体中氧气的含量.
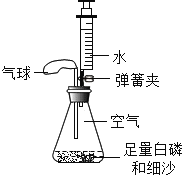
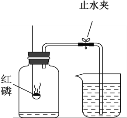
方法1:用如图B所示的装置测量气体中氧气的含量.
(1)实验前要对该装置的气密性进行检查,小明设计了一种方法,请你帮助他完成:打开止水夹,把导管末端浸没在水中,_____________,则装置气密性良好;
(2)将抽取出的气体用排水法收集到150mL的集气瓶中,关闭止水夹,点燃红磷;
(3)待装置冷却到室温后,打开止水夹,烧杯中的液体进入集气瓶中,体积约为125mL.该方法所测得氧气占气体总体积的__________%.
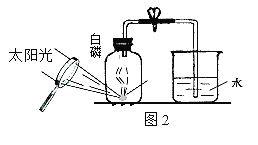
方法2:用如图C所示的装置测量气体中氧气的含量.
(1)抽取150mL的气体,缓缓地从b处通入装置中;
(2)实验结束后,c处气体的化学式为__________,集气瓶中排出液体的体积约为75mL.该方法所测得氧气约占气体总体积的__________%.
(实验反思)通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是__________(填写“方法1”或“方法2”),另一实验方法中不合理的实验操作是__________.(友情提示:请注明是哪种方法)。