题目内容
一种作为绿色能源的物质X,其燃烧的化学反应方程式:X+3O2
2CO2+3H2O 中,根据质量守恒定律判断X的化学式为( )
| ||
| A、CH3OH |
| B、CH4 |
| C、C2H5OH |
| D、H2 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答:解:由X+3O2
2CO2+3H2O可知,
反应后碳原子的个数是2个,反应前应该是2个,包含在X中;
反应后氧原子个数是7个,反应前应该是7个,其中1个包含在X中;
反应后氢原子的个数是6个,反应前应该是6个,包含在X中;
由以上分析可知,每个X中含有2个碳原子、6个氢原子和1个氧原子,是C2H5OH.
故选:C.
| ||
反应后碳原子的个数是2个,反应前应该是2个,包含在X中;
反应后氧原子个数是7个,反应前应该是7个,其中1个包含在X中;
反应后氢原子的个数是6个,反应前应该是6个,包含在X中;
由以上分析可知,每个X中含有2个碳原子、6个氢原子和1个氧原子,是C2H5OH.
故选:C.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
依据卢瑟福的原子行星模型理论,在原子中绕核高速旋转的是( )
| A、核子 | B、电子 | C、质子 | D、中子 |
下列各物质的化学式中,元素的化合价表示有错误的是( )
A、
| ||||||
B、
| ||||||
C、
| ||||||
D、
|
混合物和纯净物的主要区别是构成其分子的( )
| A、状态不同 |
| B、数量不同 |
| C、质量不同 |
| D、种类是一种还是几种 |
根据表提供的信息,下列判断正确的是( )
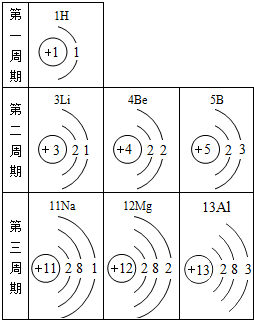

| A、元素所在的周期数等于其原子的核外电子数 |
| B、钠离子核外有三个电子层 |
| C、第二、三周期元素的原子从左至右最外层电子数逐渐增多 |
| D、在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+2 |
下列叙述中正确的是( )
| A、食盐是重要的调味品,但只有海水中含有氯化钠 |
| B、用食盐腌渍的蔬菜、鱼、肉等食品,风味独特,但不能延长保存时间 |
| C、两种盐溶液混合,不一定发生复分解反应 |
| D、某溶液能溶解铁屑,该溶液一定是酸溶液 |
