题目内容
(2010?昆山市一模)若将50g18%的NaOH溶液与50g18%的盐酸混和,下列叙述正确的是( )
【答案】分析:可以根据氢氧化钠和盐酸的反应情况进行分析、判断,从而得出正确的结论.
解答:解:由 NaOH+HCl═NaCl+H2O 可知,氢氧化钠、盐酸、氯化钠、水的质量比是:40:36.5:58.5:18.
即相同质量的HCl和NaOH反应时,NaOH完全反应,而酸剩余.
设50g18%的NaOH溶液完全反应生成的氯化钠的质量为X.
NaOH+HCl═NaCl+H2O
40 58.5
50g×18%=9g x
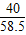 =
=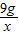
x≈13g
A、将50g18%的NaOH溶液与50g18%的盐酸混和时,盐酸过量,溶液显酸性,pH<7;
B、生成氯化钠的质量分数为: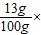 100%=13%
100%=13%
C、该反应是放热的,温度升高;
D、混合溶液的质量仍为100g.
故选D.
点评:本题主要考查了酸碱中和反应方面的问题,可以依据反应中物质的质量关系进行.
解答:解:由 NaOH+HCl═NaCl+H2O 可知,氢氧化钠、盐酸、氯化钠、水的质量比是:40:36.5:58.5:18.
即相同质量的HCl和NaOH反应时,NaOH完全反应,而酸剩余.
设50g18%的NaOH溶液完全反应生成的氯化钠的质量为X.
NaOH+HCl═NaCl+H2O
40 58.5
50g×18%=9g x
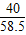 =
=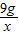
x≈13g
A、将50g18%的NaOH溶液与50g18%的盐酸混和时,盐酸过量,溶液显酸性,pH<7;
B、生成氯化钠的质量分数为:
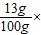 100%=13%
100%=13%C、该反应是放热的,温度升高;
D、混合溶液的质量仍为100g.
故选D.
点评:本题主要考查了酸碱中和反应方面的问题,可以依据反应中物质的质量关系进行.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
(2010?昆山市一模)下表是3种物质在不同温度时的溶解度,根据表格信息答题
(1)某饱和溶液随温度升高有固体析出,则该饱和溶液的溶质是(填化学式)
(2)要配制20℃时的NaCl饱和溶液100g,需要NaCl的质量为g(保留小数点后一位)
(3)某KNO3晶体中有少量NaCl杂质,要得到纯净KNO3的方法是:先加热溶解,然后,过滤、洗涤、干燥后得到KNO3晶体
(4)现有60℃KNO3饱和溶液210g,若加热蒸发掉10g水后恢复至60℃,析出硝酸钾晶体的质量为g.
| 温度/℃ | 20 | 40 | 60 | 80 | 100 | ||
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
| Ca(OH)2 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 |
(2)要配制20℃时的NaCl饱和溶液100g,需要NaCl的质量为g(保留小数点后一位)
(3)某KNO3晶体中有少量NaCl杂质,要得到纯净KNO3的方法是:先加热溶解,然后,过滤、洗涤、干燥后得到KNO3晶体
(4)现有60℃KNO3饱和溶液210g,若加热蒸发掉10g水后恢复至60℃,析出硝酸钾晶体的质量为g.