题目内容
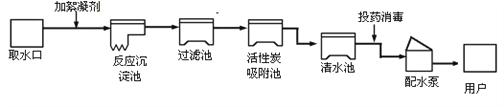
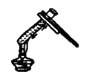
【题目】结合图示实验装置,回答下列问题。

I.(1)分别写出仪器A、B的名称;
A___________________、B__________________。
(2)小东用装置甲制取氧气,加热时发生反应的化学方程式为__________________。实验中,刚开始看到有气泡冒出时不能立即收集,原因是__________________。
(3)小明同学要制取二氧化碳,则他应该选择的装置是______ (填“甲”或“乙”),实验进行较长时间后,小明发现集气瓶中的气体仍然没有收集满,可能原因是______________________。
II.现某校研究性学习小组在老师指导下,对呼吸作用是否产生二氧化碳进行探究。
【提出问题】呼吸作用是否产生二氧化碳?
【设计方案并进行实验】
小雪:在试管中加入2mL蒸馏水,用一支玻璃导管插入水中吹气,结果未发现明显的现象。
小宁:在试管中加入2mL澄清石灰水,用玻璃导管向试管中的溶液吹气,产生的现象是:_______________,反应的化学方程式是____________________________________。
【解释与结论】根据他们的方案和实验,小宁的实验结论是______________________。
【评价与反思】小雪的方案若继续实验,也能得到小宁同样的结论。请你设计方案:
主要操作 | 预期现象 |
__________________ | ________________ |
【答案】 长颈漏斗 酒精灯 2KMnO4![]() K2MnO4 + MnO2 + O2↑ 此时排出的是装置中原有的空气 乙 装置漏气(其他合理答案也可) 澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 呼吸作用有CO2产生 向所得溶液中滴入1~2滴紫色石蕊试液 溶液变红
K2MnO4 + MnO2 + O2↑ 此时排出的是装置中原有的空气 乙 装置漏气(其他合理答案也可) 澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 呼吸作用有CO2产生 向所得溶液中滴入1~2滴紫色石蕊试液 溶液变红
【解析】I.(1)仪器A是长颈漏斗;仪器B是酒精灯;
(2)装置A适用于加热固体制取气体,并且试管口有棉团,适用于高锰酸钾制氧气,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应的化学方程式是:2KMnO4 ![]() K2MnO4+MnO2+O2↑;由于反应开始要先排出的是装置中原有的空气,刚开始看到有气泡冒出时不能立即收集;
K2MnO4+MnO2+O2↑;由于反应开始要先排出的是装置中原有的空气,刚开始看到有气泡冒出时不能立即收集;
(3)实验室制取二氧化碳用石灰石和稀盐酸,属于固+液常温下制气体,故选B装置;如果装置漏气或长颈漏斗下端没有在液面以下等都可以造成较长时间集气瓶中的气体仍然没有收集满;
II. 【设计方案并进行实验】人体呼出的气体中含有二氧化碳,二氧化碳能使澄清的石灰水变浑浊,二氧化碳和氢氧化钙反应生成水和碳酸钙,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
【解释与结论】用玻璃导管向试管中的溶液吹气时石灰水变浑浊,因为呼出的气体中含有二氧化碳,小宁的结论为:呼吸作用有CO2产生;
【评价与反思】要证明呼吸产生了二氧化碳,可以向小雪所得的溶液中加入紫色石蕊试液,观察到石蕊试液变红。

【题目】我国是一个钢铁大国,钢铁产量为世界第一。某化学实验小组的同学用下面的装置在实验室中模拟炼铁。请你和他们一起完成相关探究。
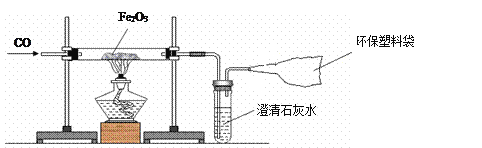
(1)操作顺序是实验成败的关键,对于该实验,应______________________(填“先通入一氧化碳”或“先点燃酒精灯”)。
(2)反应中可观察到粗玻璃管内的实验现象为__________________,写出该反应的化学方程式__________________________________________________。
(3)产物的检验:
①初步检验:甲同学想对反应后的产物进行初步检验,请你帮他想出一个物理方法:______。
②进一步验证:乙同学想用化学方法对产物进一步验证,他将反应后的黑色粉末加入足量的硫酸铜溶液中,发现只有部分变成红色。请写出生成红色物质的化学方程式:____________。
(4)质疑与探究:
①乙同学对产物的成分产生了质疑,查阅相关资料之后得知,一氧化碳还原氧化铁是一个逐渐的过程。
首先是Fe2O3被还原为Fe3O4:3Fe2O3 + CO![]() 2Fe3O4 + CO2。
2Fe3O4 + CO2。
然后是Fe3O4被还原为FeO:CO + Fe3O4![]() ______ + CO2。
______ + CO2。
最后是FeO被还原为Fe:FeO + CO ![]() Fe + CO2
Fe + CO2
②通过以上分析,甲乙两位同学对反应后黑色固体的成分进行了猜想:
已知:FeO、Fe3O4均为黑色,且Fe3O4有磁性。FeO、Fe3O4都不与硫酸铜溶液反应。
猜想一:Fe与Fe3O4; 猜想二:Fe与FeO; 猜想三:Fe与Fe3O4和FeO。
③为了对产物固体的成分进行更客观的分析,甲乙同学将所做实验整理如下:
实验内容 | 实验现象 | 实验结论 |
将反应后得到的黑色粉末 用磁铁吸引 | _____________ | 猜想一成立 |
将反应后得到的黑色粉末 加入足量的硫酸铜溶液中 | _____________ |
④实验反思:为了提高铁的产率,应适当_______(填“降低”或“提高”)反应温度。
【题目】生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.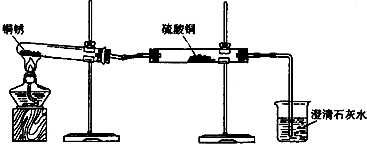
探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3 . ②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(1)【进行实验1】同学们设计了如图所示装置并进行实验.
实验橾作 | 实验现象 | 实验结论 |
①按如图组装仪器,装入药品. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有; |
③冷却后,向试管中固体 加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变 为蓝色. |
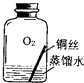
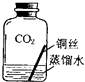
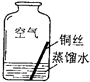
(2)【进行实验2】同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
序号 | 实验内容 | 实验结论 | 实验反思 |
实验1 |
| 在干燥环境中,铜不易生锈 | ①实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是 . |
实验2 |
| ||
实验3 |
| ||
实验4 |
| 铜生锈的条件是 |