题目内容
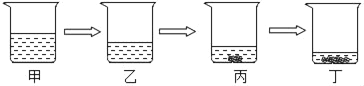
【题目】空气中氧气约占21%,利用分离液态空气的方法得到氧气是工业上制取氧气的重要途径,下面是工业上制氧气流程图:
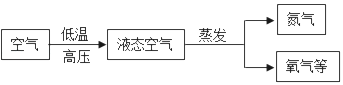
(1)工业上分离液态空气制氧气的变化属于_____(填“物理变化”或“化学变化”)。
(2)氮气的沸点﹣196℃,氧气的沸点﹣183℃,在蒸发的过程中_____(填“氮气”或“氧气”)先被蒸发出来。
(3)从微粒的角度分析,引起物质状态改变的原因是_____。
【答案】物理变化 氮气 温度升高,分子间隔变大
【解析】
(1)工业上制取氧气是利用液态氧和液态氮的沸点的不同,分离过程中没有其它物质生成,属于物理变化。
(2)氮气的沸点比氧气的沸点低,蒸发液态空气首先的到的是氮气;
(3)从微粒的角度分析,引起物质状态改变的原因是温度升高,分子间隔变大。
故答案为:
(1)物理变化;(2)氮气;(3)温度升高,分子间隔变大;

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液。同学们对该实验进行了一系列的探究。
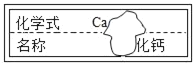
(提出问题)M溶液中的溶质是什么?
①是Ca(OH)2 ②是CaCl2
(收集资料)CaCl2水溶液呈中性
(设计实验)同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量M溶液于试管中,向其中滴入_____; | 溶液变红 | M是Ca(OH)2 |
(提出猜想)过滤后澄清滤液中含有哪些溶质
猜想一:NaOH;
猜想二:NaOH和_____;
猜想三:NaOH和Na2CO3。
(实验验证)同学们针对“猜想三”进行如下实验:
实验操作 | 实验现象 | 实验结论 |
取滤液于试管中,缓缓滴入几滴稀盐酸 | 没有气泡产生 | “猜想三”不成立 |
他们对实验结论的判断_____(填“正确”或“不正确”)。
(继续探究)设计如下实验方案确定滤液中溶质的组成:
实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中, 在A试管中加入CaCl2溶液, 在B试管中加入Na2CO3 溶液。 | 若A中产生白色沉淀,B中没有沉淀 | “猜想三”成立 |
若A中没有沉淀,B中的现象 是_____; | “猜想二”成立 | |
若A、B中都没有沉淀产生 | “猜想一”成立 |
(反思与拓展)当反应后溶液中溶质只有NaOH时说明反应物之间量的关系是_____。
【题目】 “铁丝在氧气中燃烧”的装置如图所示,回答表格中的问题。
![]()
实验步骤 | (1)预先在集气瓶中放入少量水,其作用是 。 (2)待火柴快燃尽时,再将铁丝伸入盛有氧气的集气瓶中。 “火柴快要燃尽时再伸入集气瓶中”的目的是 。 |
实验现象 | 铁丝剧烈燃烧, ,放出大量热,生成一种黑色固体。 |
实验结论 | 该反应的化学方程式是 。 |