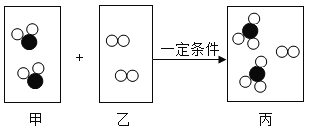
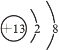题目内容
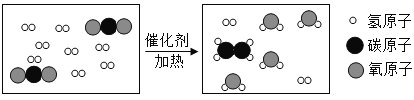
【题目】下图是实验室中常见装置,回答下列问题。
查阅资料:①常温下,CO2难溶于饱和NaHCO3溶液;②浓H2SO4能吸收CO2中的水蒸气。
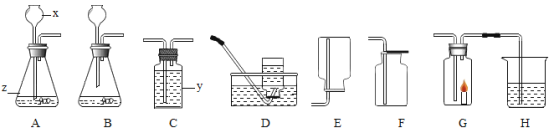
(1)写出仪器x、z的名称:x______;z_______。
(2)实验室制取CO2应选用的发生装置是______(填字母序号)反应的化学方程式是______;此装置制取气体的不足之处是______。
(3)常温下,下列收集CO2的方法中不可行的是____(填字母序号)。
a向上排空气法 b向下排空气法 c排饱和NaHCO3溶液法
(4)若要收集干燥的CO2,可将含有水蒸气的CO2通过装置C后再收集,则C中盛放的试剂y是_____。
(5)向集满CO2的集气瓶中加入澄清石灰水,反应的化学方程式为_____。
(6)某兴趣小组的同学连接A、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H 装置中溶液变浑浊,则A装置中反应的化学方程式为______。
(7)下图装置可用于气体的收集、检验、除杂和体积的测量等,不能完成的实验是_____
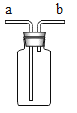
A气体从b端通入,可用于实验室收集氧气
B若瓶内为澄清石灰水,气体从b通入可检验中是否混有二氧化碳
C该装置内装水可用于医疗中给病人供氧呼吸,能观察氧气的输出速度
D收集难溶于水的气体,瓶内装满水,气体从b端通入
【答案】长颈漏斗 锥形瓶 A CaCO3+2HCl═CaCl2+CO2↑+H2O 不能控制反应的速率,浪费药品等 b 浓硫酸 CO2 +Ca(OH)2 =CaCO3↓+ H2O 2H2O2![]() 2H2O+ O2↑ AB
2H2O+ O2↑ AB
【解析】
(1)仪器x的名称是锥形瓶,仪器z的名称是长颈漏斗;
(2)实验室用大理石和盐酸反应制取二氧化碳,不需加热,属于固、液常温型,可选用发生装置A或B,B中长颈漏斗没有插入液面以下,生成的气体会逸出,实验室用大理石和盐酸反应制取二氧化碳,发生装置应选用A;大理石主要成分是碳酸钙,碳酸钙和盐酸反应生成氯化钙、水和二氧化锰,反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;装置A的缺点是不能控制反应的速率,浪费药品等;
(3)二氧化碳密度比空气大,能溶于水,可用向上排空气法收集,不可用向下排空气法;二氧化碳不能与碳酸氢钠溶液反应,能与碳酸钠反应,所以可以用排饱和碳酸氢钠溶液收集,同时又能除去二氧化碳中混有的氯化氢气体杂质,故选b;
(4)浓H2SO4能吸收CO2中的水蒸气。若要收集干燥的CO2,可将含有水蒸气的CO2通过装置C后再收集,则C中盛放的试剂y是浓硫酸;
(5)向集满CO2的集气瓶中加入澄清石灰水,氢氧化钙与二氧化碳反应生成碳酸钙和水,反应的化学方程式为CO2 +Ca(OH)2 =CaCO3↓+ H2O;
(6)某兴趣小组的同学连接A、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H 装置中溶液变浑浊,则A装置中产生了氧气,过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应的化学方程式为2H2O2![]() 2H2O+ O2↑;
2H2O+ O2↑;
(7)A 氧气的密度大于空气,氧气从a端通入集气瓶,可收集氧气,故A错误;
B、在瓶内装澄清石灰水,可检验气体中是否混有二氧化碳,气体需从a通入,故B错误;
C、瓶内装有部分水,a端接氧气钢瓶可观察是否有氧气输给病人,且能观察氧气的输出速度,故C正确;
D、瓶内装满水,气体从b端通入,可收集难溶于水的气体,故D正确。故选AB。

 阅读快车系列答案
阅读快车系列答案【题目】某品牌矿泉水的标签上标明的矿泉水主要成分如下表所示,请根据本表回答下题:
水质主要成分(mg/L) | |
偏硅酸(H2SiO3) 28.9—42.9 碳酸氢根(HCO3-) 173—205 氯(Cl-) 1.0—8.0 硫酸根(SO42-) 16.06—19.5 镁 2.5—7.5 | 锶(Sr2+) 0.01-0.32 钙 5—45 钠(Na+) 45—70 钾(K+) 0.5—2.0 pH 7.8±05 |
(1)述表格中“钙”应理解为_____(填“分子”、“原子”或“元素”);
(2)硫酸钙的化学式是_____,两个镁离子的化学符号是_____;
(3)偏硅酸(H2SiO3)中硅元素的化合价是_____;
(4)矿泉水属于_____(填“纯净物”或“混合物);
(5)下图是氧、硫、氯三种元素的粒子结构示意图。
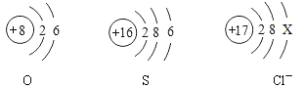
①Cl—的结构示意图中X的数值是_____;
②氧和硫两种元素的化学性质具有相似性的原因是它们原子的_____相同。