题目内容
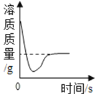
【题目】某化学小组同学为测定碳酸钙粉末与稀盐酸反应生成二氧化碳的质量(假设二氧化碳全部从溶液中逸出,不考虑试剂的挥发),进行如下实验:首先称量两个烧杯的质量(如图甲),然后将小烧杯中过量的稀盐酸倒入盛有一定量碳酸钙粉末的大烧杯中,并记录天平的示数,直至充分反应(如图乙),天平示数与反应时间的关系如图丙所示。
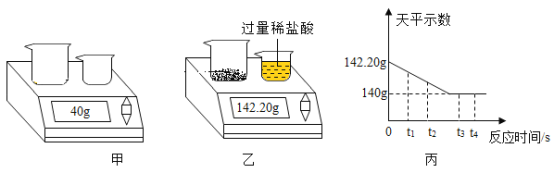
计算:(1)该反应生成的气体的质量是_____g。
(2)反应后溶液中氯化钙的质量分数_____。
【答案】2.2 5.55%
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。
(1)根据质量守恒定律,反应前物质的总质量等于生成的生成物的总质量,减少的为气体的质量,由丙图可知,反应生成的气体的质量是![]() 。
。
(2)设反应生成氯化钙的质量为x
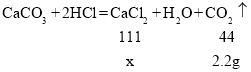
![]()
![]()
反应后溶液的溶质质量分数为![]()
答:反应后得到了![]() 的氯化钙溶液。
的氯化钙溶液。

 出彩同步大试卷系列答案
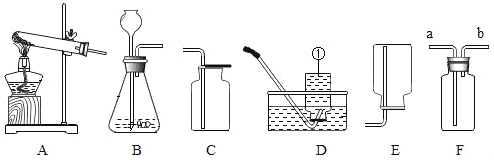
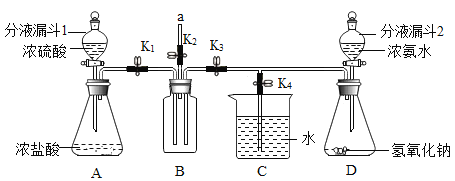
出彩同步大试卷系列答案【题目】二氧化碳与我们生活息息相关,兴趣小组利用图中装置进行多角度探究。
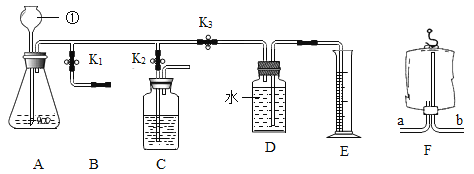
探究一 气体的制取
(1)写出图E中主要仪器的名称:__________________。
(2)用装置A制取二氧化碳的反应化学方程式是__________________。若装置A用于实验室制取氧气,则反应化学方程式是__________________。
(3)生活中有许多物品可以代替实验仪器。关闭![]() 和
和![]() ,打开
,打开![]() ,若用装置F所示的医用塑料袋排空气法收集
,若用装置F所示的医用塑料袋排空气法收集![]() ,则F装置________(填“a”或“b”)端与B装置相连。
,则F装置________(填“a”或“b”)端与B装置相连。
探究二 气体的性质检验
打开![]() 、关闭
、关闭![]() 和
和![]() ,用于检验制取的二氧化碳性质。
,用于检验制取的二氧化碳性质。
(4)若装置C中是紫色石蕊试剂,可证明二氧化碳与水发生了反应,则该反应的化学方程式是_______________。若装置C中的试剂可以检验二氧化碳,则该试剂是_____________。
探究三 测定气体生成的反应速率
关闭![]() 、
、![]() ,打开
,打开![]() ,可测一段时间内生成二氧化碳气体的速率。所测得数据如下:
,可测一段时间内生成二氧化碳气体的速率。所测得数据如下:
稀盐酸的体积(mL)(反应前) | 大理石质量(g)(反应前) | E装置收集的液体量(mL) | 反应时间(s) |
50 | 5.0 | 37.8 | 100 |
(5)由实验数据可知,生成![]() 的体积为___________
的体积为___________![]() 。
。
(6)若生成气体的反应速率用公式![]() 表示(
表示(![]() 表示生成气体的体积、
表示生成气体的体积、![]() 表示反应所用的时间),则生成的二氧化碳的速率为_________
表示反应所用的时间),则生成的二氧化碳的速率为_________![]() 。
。
(7)有同学认为,图中的测量方法容易带来误差,请指出造成误差的原因___________________(写一点)。