题目内容
【题目】如图是干电池的截面示意图。废旧电池也是资源,将其回收利用对保护环境具有重要意义。结合示意图回答下列问题
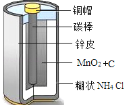
(1)碳棒(主要成分是石墨)用作电极,是利用石墨的_____性。
(2)将电池填充物(MnO2、C及NH4Cl的混合物)加水溶解、过滤,可得到NH4Cl溶液。NH4Cl还可用作化肥使用,属于化肥中的_____肥。
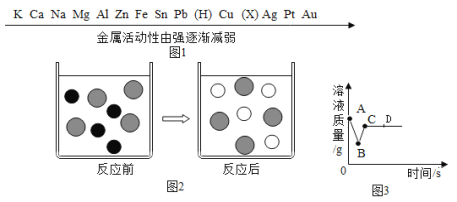
(3)干电池中含有金属铜和锌,以下能证明铜、锌金属活动性强弱的试剂组合是_____(填序号)。
A锌、铜和稀硫酸 B锌和氯化铜溶液 C铜和硫酸锌溶液
(4)将mgZn和Fe的混合物加入到一定质量的CuCl2溶液中,充分反应后过滤,将滤渣洗涤、干燥后称量。质量仍为mg,对所得滤液和滤渣有如下四种判断:
A滤液可能是无色 B滤液中一定有ZnCl2和FeCl2
C滤渣中的物质可能有3种 D滤渣中加稀盐酸一定有气泡产生
以上判断正确的是_____(填序号)
【答案】导电 氮 ABC B
【解析】
(1)碳棒(主要成分是石墨)用作电极,是利用石墨的导电性。故填:导电。
(2)NH4Cl中含有氮元素,可用作化肥使用,属于化肥中的氮肥。故填:氮。
(3)A、把锌、铜分别加入稀硫酸中时,锌表面产生气泡,铜表面无明显现象,说明锌比铜活泼;
B、把锌放入氯化铜溶液中时,锌表面附着红色固体,说明锌比铜活泼;
C、铜和硫酸锌溶液混合时,无明显现象,说明锌比铜活泼。
故选:ABC。
(4)锌、铁和氯化铜反应的化学方程式及其质量关系为:
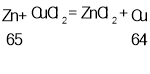
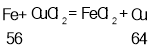
由以上质量关系可知,锌和氯化铜反应时固体质量减小,铁和氯化铜反应时固体了增大;
A、将滤渣洗涤、干燥后称量。质量仍为mg,说明锌已经完全反应,铁已经反应,生成氯化亚铁(浅绿色),因此滤液不可能是无色的,该选项说法不正确;
B、将滤渣洗涤、干燥后称量。质量仍为mg,说明锌已经完全反应,铁已经反应,因此滤液中一定有锌和氯化铜反应生成的氯化锌ZnCl2和铁与氯化铜反应生成的FeCl2,该选项说法正确;
C、滤渣中的物质一定有铜,可能有铁,一定不含锌,因此不可能有3种,该选项说法不正确;
D、滤渣中如果含有铁,则加稀盐酸有气泡产生,如果不含有铁,加入稀盐酸时不产生气泡,该选项说法不正确。
故选:B。

【题目】下列4个图像中,能正确反映对应变化关系的是
|
|
|
|
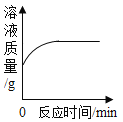
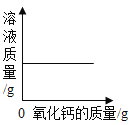
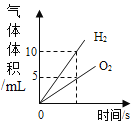
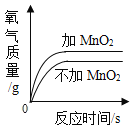
A向一定量的硝酸银溶液中插入铜丝 | B向一定量的饱和石灰水中加入氧化钙 | C将水通电电解一段时间 | D两份等体积的5%过氧化氢溶液,向其中一份加入少量MnO2 |
A.AB.BC.CD.D