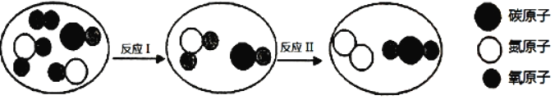
��Ŀ����
����Ŀ��ij��ȤС��ͬѧ��CuSO4��Һ��NaOH��Һ��Ӧ���ɵ���ɫ�������������̽����
��1��д��������ɫ�����ķ�Ӧ����ʽ______��
��2������ɫ�������м��ȣ�һ�㿴����ɫ�������ɫ������ʱȴ������ɫ��������ɫ������ȤС������쳣�����������Ȥ�������������������ʵ����������̽����
���������ϣ������Լ������ֽ�ɶ�Ӧ�Ľ��������д����ɫ�������ɫ�Ļ�ѧ����ʽ______��
��������⣩������ɫ���������ֺ�ɫ��������ʲô�����йأ�
���������룩����һ��������ͭ��Һ�����й�
�������������������Һ�����й�
�����ʵ�飩��ѡ�Լ���1%��NaOH��Һ��20%��NaOH��Һ��20%��CuSO4��Һ��1%��CuSO4��Һ��
ʵ����� | ʵ������ | ʵ����� |
��1�� ______ �ٽ����ó������� | �Ȳ�����ɫ���������Ⱥ� ______ | ����һ������ |
��2����2mL20%NaOH��Һ�еμ�2��1%CuSO4��Һ���ٽ����ó������� | ______ | ��������� |
��ʵ����ۣ�������ʵ���У�Ҫ�ܹ۲쵽��ɫ�������ɫ�Ĺؼ���______��
����չ���죩��һ���������Ͽ�֪������ɫ�������ܽ�ȱ�������ͭ��С�ļ�ʽ����ͭ[��ѧʽΪCu4��OH��6SO4]���ڼ��Խ�ǿ�������������γɣ���������һ��ʱ�����ɫ������ɲ�����ɫ�����������һ��ʵ�飬֤����dz��ɫ�����к������������______��
���𰸡�CuSO4+2NaOH=Cu��OH��2��+Na2SO4 Cu��OH��2![]() CuO+H2O ��2mL20%CuSO4��Һ�еμ�2��l% NaOH��Һ ��ɫ�������ɫ �Ȳ�����ɫ���������Ⱥ���ɫ������Ϊ��ɫ CuSO4Ҫ��������NaOH���㣩 ��dz��ɫ����Һ���ˣ����ѵõ�����ɫ����������ˮ���ϴ�ӣ���ϴ��Һ����BaCl2��Һ���鲻��SO42-����ϡ�����ܽ���ɫ��������ʱ����BaCl2��Һ���飬�ܽ�Һ���д�����ɫBaSO4���ɣ���ʾdz��ɫ��������SO42-
CuO+H2O ��2mL20%CuSO4��Һ�еμ�2��l% NaOH��Һ ��ɫ�������ɫ �Ȳ�����ɫ���������Ⱥ���ɫ������Ϊ��ɫ CuSO4Ҫ��������NaOH���㣩 ��dz��ɫ����Һ���ˣ����ѵõ�����ɫ����������ˮ���ϴ�ӣ���ϴ��Һ����BaCl2��Һ���鲻��SO42-����ϡ�����ܽ���ɫ��������ʱ����BaCl2��Һ���飬�ܽ�Һ���д�����ɫBaSO4���ɣ���ʾdz��ɫ��������SO42-
��������
��1����Ӧ��������ͭ���������ƣ���������������ͭ�������ƣ���Ӧ�Ļ�ѧ����ʽΪ��CuSO4+2NaOH=Cu��OH��2��+Na2SO4��
[��������]��Ӧ����������ͭ��������������ͭ��ˮ����Ӧ�����Ǽ��ȣ���Ӧ�Ļ�ѧ����ʽΪ��Cu��OH��2![]() CuO+H2O��
CuO+H2O��
[���ʵ��]��2mL20%NaOH��Һ�еμ�2��1%����ͭ��Һ���ٽ����ó������ȣ�ʵ����۵ó���NaOH��Һ�����йأ���˶�Ӧ��ʵ���������Ȳ�����ɫ���������Ⱥ���Ⱥ���ɫ������Ϊ��ɫ������ʵ�鷽��2�����ʵ�鷽��1����2mL20%CuSO4��Һ�еμ�2��l%NaOH��Һ���ٽ����ó������ȣ�ʵ����۵ó���CuSO4��Һ�����أ���˶�Ӧ��ʵ�������Ǽ��Ⱥ���ɫ�������ɫ��
[ʵ�����]������ʵ�鷽���Աȵó�����ɫ�������ɫ��ԭ����CuSO4��Һ������NaOH��Һ�������㣻
[��չ�뷴˼]��dz��ɫ����Һ���ˣ����ѵõ�����ɫ����������ˮ���ϴ�ӣ���ϴ��Һ����BaCl2��Һ���鲻��SO42-����ϡ�����ܽ���ɫ��������ʱ����BaCl2��Һ���飬�ܽ�Һ���д�����ɫBaSO4���ɣ���ʾdz��ɫ��������SO42-��

 ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д� Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д� ������������Ծ�ϵ�д�
������������Ծ�ϵ�д�