题目内容
【题目】取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸。实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图所示。(资料酸钠与稀盐酸反应分两步进行:Na2CO3+HCl=NaHCO3+NaCl, NaHCO3+HCl=NaCl+H2O+CO2↑)下列说法正确的是 ( )
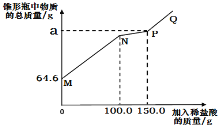
A. N点的溶液表示氢氧化钠被恰好完全反应
B. PQ段(不含P点)溶液的pH<7
C. NP段表示产生气体的过程,a的值为210.2
D. 该固体样品中氢氧化钠的质量为8.0g
【答案】B.C
【解析】
试题分析∶酸钠与稀盐酸反应分两步进行:MN段∶Na2CO3+HCl=NaHCO3+NaCl, NP段∶ NaHCO3+HCl=NaCl+H2O+CO2↑ PQ段稀盐酸过量,溶液的pH<7,故B正确。A. 稀盐酸应先与氢氧化钠反应,N点的溶液表示NaHCO3+HCl=NaCl+H2O+CO2↑恰好反应完,故A错误。C.根据关系式HCL→
NaCL,可算出 a的值为210.2,故C正确。D.根据有关方程式可算出固体样品中氢氧化钠的质量,不是8.0g,故D错误。
考点∶考查根据化学方程式进行有关计算。

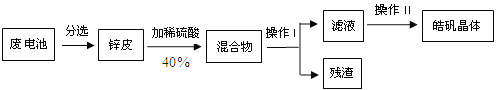
【题目】石膏法制取硫酸钾具有能耗低,原料来源广等优点而被探索。以硫酸钙与氯化钾为原料制备硫酸钾的流程如下:
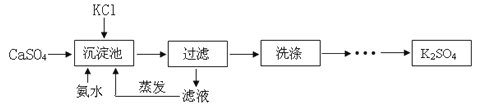
已知硫酸钾在不同温度下在水溶液、氨溶液中的溶解度(g)
温度(℃) | 0 | 10 | 26 | 30 |
水溶液 | 7.31 | 9.28 | 11.03 | 12.98 |
氨(8%)溶液 | 1.41 | 1.58 | 2.25 | 3.36 |
氨(35%)溶液 | 0.44 | 0.75 | 0.82 | 非常压 |
(1)氨水显 (填“酸性”、“碱性”或“中性”),向水中连续通氨气达两个小时可得高浓度氨水,氨气不断溶解使溶液pH (填“增大”、“减小”或“不变”)。上表中“非常压”指需增大气压才能形成30℃的氨(35%)溶液,常压下不能形成30℃的氨(35%)溶液的原因是 。
(2)沉淀池中氨水浓度常常控制在25%至40%,其原因是 ,沉淀池温度适宜保持在
(选填“低温”或“高温”)。
(3)滤液经蒸发后产生可以循环使用的气体,其化学式为 ;滤液中的副产品氯化钙可转化成碳酸钙固体,与HNO3反应制备Ca(NO3)2·6H2O晶体,为确保制备过程中既不补充水,也无多余的水,所用硝酸溶液中溶质与溶剂的质量比为 。
(4)实验室进行过滤操作需要的玻璃仪器有烧杯、玻璃棒、 ,其中玻璃棒在稀释浓硫酸时也用到,稀释浓硫酸时用到玻璃棒的主要作用为 。
(5)检验沉淀是否洗净的试剂是 (填序号)
A.酚酞试液 B碳酸钠溶液 C氯化钡溶液