题目内容
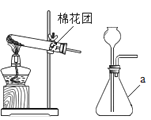
【题目】小刚同学在实验室中对一种紫褐色固体粉末A进行探究实验,他实验的过程和现象如下,请你根据上实验探究,回答下列问题:
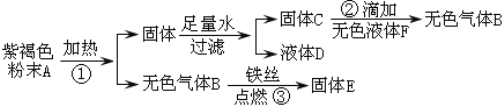
(1)A物质的名称为:______
(2)写出B的一种用途:______。
(3)反应③的文字表达式为:______
(4)反应③的反应现象为______。
(5)反应③的基本反应类型为:______。
【答案】高锰酸钾 供给呼吸、支持燃烧 铁+氧气![]() 四氧化三铁 剧烈燃烧,火星四射,放出大量热,生成黑色固体 化合反应
四氧化三铁 剧烈燃烧,火星四射,放出大量热,生成黑色固体 化合反应
【解析】
(1)无色气体B和铁丝点燃会生成E,所以B是氧气,E是四氧化三铁,紫褐色的粉末A加热会生成氧气,所以A是高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,固体C中滴加F也会生成氧气,所以C是二氧化锰,D是锰酸钾,F是过氧化氢溶液,经过验证,推导正确,所以A是高锰酸钾;
(2)通过推导可知,B是氧气,可以供给呼吸;
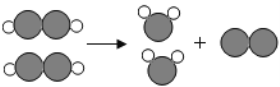
(3)反应③是铁和氧气在点燃的条件下生成四氧化三铁;
(4)反应③是铁和氧气在点燃的条件下生成四氧化三铁,反应现象为:剧烈燃烧,火星四射,放出大量热,生成黑色固体;
(4)反应③满足多变一的条件,属于化合反应.
故答案为:(1)高锰酸钾;
(2)供给呼吸;
(3)铁+氧气![]() 四氧化三铁;
四氧化三铁;
(4)剧烈燃烧,火星四射,放出大量热,生成黑色固体;
(5)化合反应.

 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】在小英家的仓库里,堆放着一袋袋化肥一一碳酸氢铵( NH4HCO3).过了一个夏天,小英发现这种化肥所持有的刺激性气味变得更浓烈了,有些化肥袋里碳酸氢铵变少了,检查发现变少的化肥包装袋没有密封,化肥也没有撒落在地上,更没有人进过仓库开袋使用。
为了探究这些化肥减少的原因,小英在实验室取了一些碳酸氢铵粉末,放在蒸发皿中加热,过一会儿观察到粉末完全消失,同时也闻到了这种刺激性气味.粉末为什么会消失呢?
(1)(提出问题)碳酸氢铵粉末消失的原因是什么?
(2)(猜想)①碳酸氢铵粉末在不加热或加热条件下由固态变成它的气态。②碳酸氢铵在不加热或加热条件下发生分解反应,可能产生的物质有氨气和一些氧化物。
(3)(查阅资料)①碳酸氢铵属于氨肥,不具有升华的性质,说明上述猜想__________ (填序号)不成立;②氨气(化学式NH3)具有特殊的刺激性气味,极易溶于水,其水溶液是碱性,但干燥的氨气不能使干燥的红色石蕊试剂变蓝;③NO2为红棕色气体。NO为无色气体,在空气中易发生反应:2NO+O2=2NO2
(4)(实验操作,现象与结论)
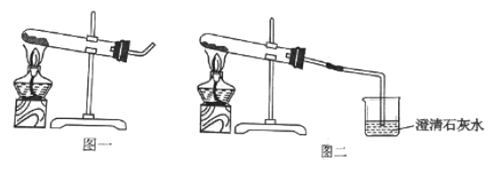
实验操作 | 实验现象 | 实验结论 |
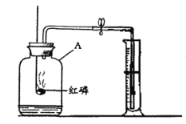
①取适量碳酸氢铵于试管中加热,如图一所示,将干燥的红色石蕊试纸接近导管口 | 产生强烈的刺激性气味,试管壁上有无色液滴且试纸变蓝,但未见红棕色气体 | 分解产物中有______,没有__________ |
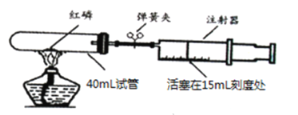
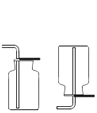
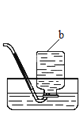
②按如图二所示装置继续实验,直到反应完全 | 澄清石灰水变浑浊 | 分解产物中有__________ |
(5)(应用)①利用氨气的化学性质,请写出实验室检验氨气的方法(写出实验操作、现象、结论):________________________________________;
②如果你家里有碳酸氢铵化肥,你应该如何保存? ______________________________。