题目内容
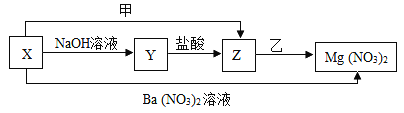
【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性。他们经过思考设计并进行了以下实验:

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含____________,可能含有____________。
(2)生成白色沉淀的化学方程式为________________________________________________。
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
[提出问题]无色滤液中呈碱性的物质是什么?
[做出猜想]猜想Ⅰ:Na2CO3;猜想Ⅱ:①____________;猜想Ⅲ:Na2CO3和NaOH。
[进行实验]
实验步骤 | 实验现象 | 结论 |
1.取少许该溶液于试管中,滴入②___________溶液。 | ③___________________ | 猜想三正确 |
2.静置上述溶液,取上层清液少许于另一支试管中,滴入几滴④___________溶液。 | ⑤___________________ |
[得出结论]白色粉末的成分是⑥____________。
【答案】 CuSO4 、Na2SO4 NaOH BaCl2+Na2CO3=BaCO3↓+2 NaCl. NaOH 氯化钡 产生白色沉淀 无色酚酞 溶液变红色 Na2CO3、BaCl2、NaOH。
【解析】由题中信息知,加入水得无色溶液和白色沉淀,一定没有硫酸铜。白色沉淀加入足量稀盐酸,沉淀全部溶解,一定没有Na2SO4。 无色溶液呈碱性,可能含有氢氧化钠,碳酸钠溶液呈碱性。(1)白色粉末中一定不含CuSO4 、Na2SO4 。可能含有NaOH。(2)生成白色沉淀的化学方程式为BaCl2+ Na2CO3=Ba CO3↓+2 NaCl. (3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。[提出问题]无色滤液中呈碱性的物质是什么?[做出猜想]猜想Ⅰ:Na2CO3;猜想Ⅱ:①. NaOH ;猜想Ⅲ:Na2CO3和NaOH。[进行实验]
实验步骤 | 实验现象 | 结论 |
1.取少许该溶液于试管中,滴入②氯化钡 溶液。 | ③产生白色沉淀。 | 猜想三正确 |
2.静置上述溶液,取上层清液少许于另一支试管中,滴入几滴④无色酚酞溶液。 | ⑤溶液变红色 |
[得出结论]白色粉末的成分是Na2CO3、BaCl2、NaOH。
点睛∶本题主要考查物质成分的鉴别以及实验探究的基本思路和方法。

 名校课堂系列答案
名校课堂系列答案