题目内容
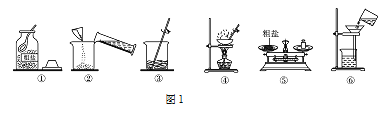
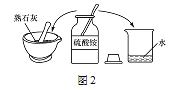
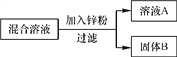
【题目】某化学小组用一定量的AgNO3和Cu(NO3)2的混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和研究。
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】
①只有Zn(NO3)2;
②Zn(NO3)2、AgNO3;
③Zn(NO3)2、Cu(NO3)2;
④Zn(NO3)2、Cu(NO3)2、AgNO3。
【交流讨论】不合理的猜想是________(填标号),其理由是____________________________。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现象 | 结论 |
取少量固体B,滴加________(填试剂名称) | 有气泡 产生 | 固体B的成分为________,有关反应的化学方程式为___________________________ |
【答案】 ② 猜想②中无Cu(NO3)2,说明Cu(NO3)2已与Zn反应生成Cu,而Cu能与AgNO3反应,所以不可能只有AgNO3存在而无Cu(NO3)2存在 稀盐酸 锌、铜、银 Zn+2HCl===ZnCl2+H2↑
【解析】试题分析:向AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,因锌的活动性强与铜和银,而铜的活动性强于银,则锌将置换AgNO3中的银,也会置换Cu(NO3)2中的铜,而铜又将置换AgNO3中的银。
1、若锌是适量或过量的的,则反应后,溶液A中只有Zn(NO3)2;若锌较少,只反应了AgNO3,则溶液A中有Zn(NO3)2、Cu(NO3)2;若锌太少,则溶液A中有 Zn(NO3)2、Cu(NO3)2、AgNO3;题中②的猜想是不合理的,因为猜想②中无硝酸铜,说明Cu(NO3)2已与锌反应生成Cu,而铜能与硝酸银反应,所以不可能存在硝酸银。
2、若猜想①成立,则锌可能是恰好反应,也可能是过量,有剩余。则:取少量固体B,滴
加稀盐酸,若有气泡产生,则锌是过量的,固体B的成分为Zn、Cu、Ag,因Cu、Ag的活动性弱于H,故有关的化学方程式为:Zn+2HCl═ZnCl2+H2↑ 。

 名校课堂系列答案
名校课堂系列答案【题目】某校同学开展了如下“溶液酸碱性的检验”的实验活动:
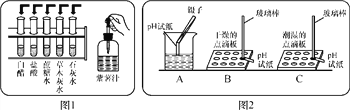
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁 后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称:________;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是________;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于________(填“酸性”“中性”或“碱性”)溶液,白醋pH________(填“>”“<”或“=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是________(填“A”“B”或“C”,下同),可能导致被测溶液pH数值发生改变的错误操作是________。