题目内容
(2005?湘潭)下面是金属钠与水反应的实验记录,请仔细阅读后回答下列问题:从煤油中取出一块金属钠,用滤纸吸干净表面的煤油后,用小刀切下一小块.切口呈现出银白色的金属光泽,光泽迅速消失、变暗,原因是钠与空气中的氧气迅速反应.将这小块钠投入水中,钠浮于水面,剧烈反应,急速游动,并熔成一个闪亮的小球,逐渐缩小,最后完全消失.向反应后的溶液中滴加2滴无色酚酞试液,溶液变红色.
(1)金属钠具有哪些物理性质?
(2)金属钠与水的反应(2Na+2H2O═2NaOH+H2↑)属于
(3)反应后的溶液pH
(4)金属钠通常必须保存在煤油中,原因是金属钠易与
(5)小明同学通过对以上内容的学习,结合所学习的化学知识推断出金属钠的金属活动性比铁活泼.他推断的依据是什么?
(1)金属钠具有哪些物理性质?
是一种固体金属;有银白色金属光泽;密度比水小;质软(硬度小);熔点低
是一种固体金属;有银白色金属光泽;密度比水小;质软(硬度小);熔点低
.(2)金属钠与水的反应(2Na+2H2O═2NaOH+H2↑)属于
置换
置换
反应.(填“分解”“化合”“置换”“复分解”)(3)反应后的溶液pH
>
>
7,(填“>”“<”“=”)原因是反应生成了NaOH
NaOH
.(4)金属钠通常必须保存在煤油中,原因是金属钠易与
空气中的氧气或与空气中的水
空气中的氧气或与空气中的水
发生反应.(5)小明同学通过对以上内容的学习,结合所学习的化学知识推断出金属钠的金属活动性比铁活泼.他推断的依据是什么?
分析:物质的物理性质指不需要发生化学变化就表现出来的性质;置换反应的要点是一种单质和一种化合物反应生成另一种单质和另一种化合物;钠的保存需要考虑钠的性质;通过钠与空气和水发生反应的现象,可得钠比铁活泼.
解答:解:(1)物质的物理性质指不需要发生化学变化就表现出来的性质,状态、颜色、硬度、密度、熔点等都属于物理性质,能用刀切说明硬度小,能浮于水面说明密度比水小,熔成一个闪亮的小球说明熔点低;
(2)置换反应的要点是一种单质和一种化合物反应生成另一种单质和另一种化合物,故属于置换反应;
(3)因为钠与水反应生成了氢氧化钠,氢氧化钠属于碱,故溶液的pH>7;
(4)钠与空气中的氧气和水会迅速反应,很活泼,故保存在煤油里可以隔绝氧气和水;
(5)钠可以迅速与空气,水发生反应,而铁却不能,所以比铁活泼.
故答案为:
(1)是一种固体金属;有银白色金属光泽;密度比水小;质软(硬度小);熔点低.
(2)置换;
(3)>;NaOH;
(4)与空气中的氧气或与空气中的水;
(5)钠能与水反应,而铁不能,说明钠比铁活泼.
(2)置换反应的要点是一种单质和一种化合物反应生成另一种单质和另一种化合物,故属于置换反应;
(3)因为钠与水反应生成了氢氧化钠,氢氧化钠属于碱,故溶液的pH>7;
(4)钠与空气中的氧气和水会迅速反应,很活泼,故保存在煤油里可以隔绝氧气和水;
(5)钠可以迅速与空气,水发生反应,而铁却不能,所以比铁活泼.
故答案为:
(1)是一种固体金属;有银白色金属光泽;密度比水小;质软(硬度小);熔点低.
(2)置换;
(3)>;NaOH;
(4)与空气中的氧气或与空气中的水;
(5)钠能与水反应,而铁不能,说明钠比铁活泼.
点评:考查了物理性质和化学性质的判断,反应类型的判定,金属的活动性顺序及金属的保存等.金属的保存需要考虑金属的物理性质和化学性质.

练习册系列答案
相关题目
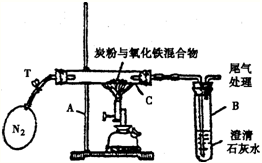 (2005?湘潭)某化学兴趣小组的学生研究过量的碳粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:
(2005?湘潭)某化学兴趣小组的学生研究过量的碳粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下: