题目内容
26、根据下列制取氧气的装置图回答问题.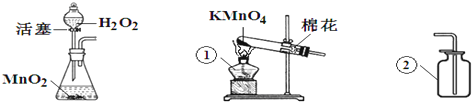
(1)写出仪器①、②的名称①
(2)实验室常用高锰酸钾或过氧化氢和二氧化锰来制取氧气,你认为其中相对较好的方法是
(3)可以
(4)何洁同学在制取氧气过程中,她收集一瓶氧气后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃.其原因可能是
(5)若用排水法收集氧气,则导管口开始有气泡放出时,不宜立即收集,因为

(1)写出仪器①、②的名称①
酒精灯
;②集气瓶
.(2)实验室常用高锰酸钾或过氧化氢和二氧化锰来制取氧气,你认为其中相对较好的方法是
过氧化氢和二氧化锰来制取氧气
,其理由是不需加热(或可以控制反应速率或生成物对环境没有污染)
.(3)可以
向上
用排空气法收集氧气,原因是氧气的密度大于空气
,检验集气瓶中是否收集满氧气的方法是,将带火星的小木条放在集气瓶口
,若木条复燃
,说明已满.(4)何洁同学在制取氧气过程中,她收集一瓶氧气后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃.其原因可能是
装置气密性不好(或用错药品或药品变质或收集的时间不够长)
.(5)若用排水法收集氧气,则导管口开始有气泡放出时,不宜立即收集,因为
在制取氧气的装置中有空气,则开始排出的气体中混有空气,若一开始就收集则氧气中混有空气使氧气不纯
.实验即将结束时,应先先把导管从水槽中拿出
,后熄灭酒精灯
,否则会导致水槽中的水倒流入试管,使试管炸裂
.分析:(1)掌握常用仪器的名称,即可得出答案.
(2)分析比较实验室用高锰酸钾和用过氧化氢和二氧化锰来制取氧气的优缺点;
(3)根据气体的性质选择收集和验满方法;
(4)分析实验中常出现的一种现象,收集的氧气不能使带火星的木条复燃;
(5)收集气体不要立即收集,否则收集到的气体不纯,完毕后先撤导管后熄灭酒精灯;
(2)分析比较实验室用高锰酸钾和用过氧化氢和二氧化锰来制取氧气的优缺点;
(3)根据气体的性质选择收集和验满方法;
(4)分析实验中常出现的一种现象,收集的氧气不能使带火星的木条复燃;
(5)收集气体不要立即收集,否则收集到的气体不纯,完毕后先撤导管后熄灭酒精灯;
解答:解:(1)熟记常见仪器,即可得出答案:①酒精灯;②集气瓶;
(2)实验室用高锰酸钾和用过氧化氢和二氧化锰来制取氧气,其中用过氧化氢和二氧化锰制取氧气优点更多,即不需加热;可以控制反应速率;生成物对环境没有污染等;
(3)因氧气密度比空气的密度大,应选向上排空气法收集;氧气具有助燃性,验满时要用带火星木条,并将其放到集气瓶瓶口,若木条复燃,说明已满;
(4)收集的氧气,用带火星的木条伸入瓶口、瓶中、瓶底,木条都不能复燃,可能的原因有:装置气密性不好;用错药品或药品变质;收集的时间不够长(任答一条即可,其他合理答案均可)
(5)在制取氧气的装置中有空气,则开始排出的气体中混有空气,若一开始就收集则氧气中混有空气使氧气不纯;
实验完毕如果先熄灭酒精灯,试管内压强减小,水会沿着导管倒吸入试管内,使试管炸裂,所以要先撤导管后熄灭酒精灯.
故答案为:
(1)①酒精灯;②集气瓶;
(2)过氧化氢和二氧化锰来制取氧气,装置气密性不好,用错药品或药品变质,收集的时间不够长(任答一条即可,其他合理答案均可);
(3)向上,氧气密度大于空气,集气瓶口,复燃;
(4)装置气密性不好;用错药品或药品变质;收集的时间不够长(任答一条即可,其他合理答案均可);
(5)此时排出的是空气;先把导管从水槽中拿出;熄灭酒精灯,水槽中的水倒流入试管,使试管炸裂.
(2)实验室用高锰酸钾和用过氧化氢和二氧化锰来制取氧气,其中用过氧化氢和二氧化锰制取氧气优点更多,即不需加热;可以控制反应速率;生成物对环境没有污染等;
(3)因氧气密度比空气的密度大,应选向上排空气法收集;氧气具有助燃性,验满时要用带火星木条,并将其放到集气瓶瓶口,若木条复燃,说明已满;
(4)收集的氧气,用带火星的木条伸入瓶口、瓶中、瓶底,木条都不能复燃,可能的原因有:装置气密性不好;用错药品或药品变质;收集的时间不够长(任答一条即可,其他合理答案均可)
(5)在制取氧气的装置中有空气,则开始排出的气体中混有空气,若一开始就收集则氧气中混有空气使氧气不纯;
实验完毕如果先熄灭酒精灯,试管内压强减小,水会沿着导管倒吸入试管内,使试管炸裂,所以要先撤导管后熄灭酒精灯.
故答案为:
(1)①酒精灯;②集气瓶;
(2)过氧化氢和二氧化锰来制取氧气,装置气密性不好,用错药品或药品变质,收集的时间不够长(任答一条即可,其他合理答案均可);
(3)向上,氧气密度大于空气,集气瓶口,复燃;
(4)装置气密性不好;用错药品或药品变质;收集的时间不够长(任答一条即可,其他合理答案均可);
(5)此时排出的是空气;先把导管从水槽中拿出;熄灭酒精灯,水槽中的水倒流入试管,使试管炸裂.
点评:此题考查氧气的实验装置制法的原理,制取的优缺点,误差分析等,应知道比较装置优缺点时的几个方面.

练习册系列答案
 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目


 过碳酸钠固体是过氧化氢和碳酸钠加合而成的化合物.其化学式为2Na2CO3?3H2O2,有关该化合物叙述如下.
过碳酸钠固体是过氧化氢和碳酸钠加合而成的化合物.其化学式为2Na2CO3?3H2O2,有关该化合物叙述如下.