题目内容
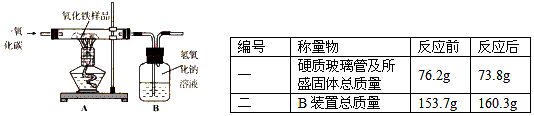
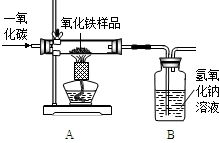 现有一种不纯的氧化铁粉末样品(杂质为铁粉),小刚和小强通过实验测定样品中氧化铁的质量分数.请你回答相关问题:
现有一种不纯的氧化铁粉末样品(杂质为铁粉),小刚和小强通过实验测定样品中氧化铁的质量分数.请你回答相关问题:(1)小刚称取10g样品,利用下图所示装置进行实验,相关实验数据见下表:(玻璃管内的物质完全反应)
| 编号 | 称量物 | 反应前 | 反应后 |
| 一 | 硬质玻璃管及所盛固体总质量 | 76.2g | 73.8g |
| 二 | B装置总质量 | 153.7g | 160.3g |
②请根据B装置总质量变化的数据,计算出样品中氧化铁的质量分数(写出计算过程).
解:设样品中氧化铁的质量为x.
(2)为达到同样的实验目的,小强设计的方案为:将一定质量的样品于过量的稀盐酸反应,准确称量反应前、后固体和液体物质的总质量,据此可求出氧化铁的质量分数.
请你分别对小刚和小强设计的实验方案进行评价(各写出一条即可):
(3)如果小强还想计算出所用稀盐酸的溶质质量分数,请简要说明对其方案的改进方法及原因:
分析:(1)①根据反应前后玻璃管中物质的种类进行分析.
②B装置前后增加的是二氧化碳的质量,可利用一氧化碳和氧化铁反应的化学方程式,根据二氧化碳的质量求出氧化铁的质量,再根据
×100%求出样品中氧化铁的质量分数.
(2)从操作是否简单、实验结果是否准确、实验是否容易控制、是否会造成污染等角度进行分析.
(3)要求稀盐酸中溶质的质量分数,必须要知道参加反应的稀盐酸中溶质的质量和恰好完全反应时所用的稀盐酸的质量.溶质的质量可根据氢气的质量和氧化铁的质量计算出来,而恰好完全反应时所用的稀盐酸的质量并不知道,小强设计的方案中所用的盐酸是过量的,所以应加盐酸至恰好完全反应.
②B装置前后增加的是二氧化碳的质量,可利用一氧化碳和氧化铁反应的化学方程式,根据二氧化碳的质量求出氧化铁的质量,再根据
| 氧化铁的质量 |
| 样品的质量 |
(2)从操作是否简单、实验结果是否准确、实验是否容易控制、是否会造成污染等角度进行分析.
(3)要求稀盐酸中溶质的质量分数,必须要知道参加反应的稀盐酸中溶质的质量和恰好完全反应时所用的稀盐酸的质量.溶质的质量可根据氢气的质量和氧化铁的质量计算出来,而恰好完全反应时所用的稀盐酸的质量并不知道,小强设计的方案中所用的盐酸是过量的,所以应加盐酸至恰好完全反应.
解答:解:(1)①反应前玻璃管中的物质是氧化铁和铁粉,反应后玻璃管中的物质是铁粉,可知玻璃管中的物质前后减少的质量是氧元素的质量.故答案为:氧元素
②反应后生成二氧化碳的质量为:160.3g-153.7g=6.6g
设样品中氧化铁的质量为x
3CO+Fe2O3
2Fe+3CO2
160 132
x 6.6g
=
x=8g
样品中氧化铁的质量分数为
×100%=80%
答:样品中氧化铁的质量分数为80%.
(2)小刚:若用玻璃管质量变化值计算氧化铁质量,数据准确;使用一氧化碳,具有一定危险性
小强:不需要加热,操作简便;不易控制盐酸是否完全反应
(3)应改为向一定质量的样品中加入稀盐酸至恰好完全反应,测量所用稀盐酸的质量.
小强设计的方案中所加的稀盐酸是过量的,而要求稀盐酸中溶质的质量分数必须要知道稀盐酸中溶质的质量和所用稀盐酸的质量.
②反应后生成二氧化碳的质量为:160.3g-153.7g=6.6g
设样品中氧化铁的质量为x
3CO+Fe2O3
| ||
160 132
x 6.6g
| 160 |
| 132 |
| x |
| 6.6g |
样品中氧化铁的质量分数为
| 8g |
| 10g |
答:样品中氧化铁的质量分数为80%.
(2)小刚:若用玻璃管质量变化值计算氧化铁质量,数据准确;使用一氧化碳,具有一定危险性
小强:不需要加热,操作简便;不易控制盐酸是否完全反应
(3)应改为向一定质量的样品中加入稀盐酸至恰好完全反应,测量所用稀盐酸的质量.
小强设计的方案中所加的稀盐酸是过量的,而要求稀盐酸中溶质的质量分数必须要知道稀盐酸中溶质的质量和所用稀盐酸的质量.
点评:本道题是一道实验与计算相结合的综合题,既要根据实验测量数据进行计算,还要设计实验测量出稀盐酸中溶质的质量分数,是一道考查学生用所学知道解决实际生活问题能力的题.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
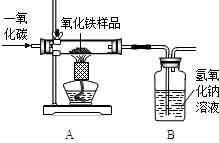 现有一种不纯的氧化铁粉末样品(杂质为铁粉),小刚和小强通过实验测定样品中氧化铁的质量分数.请你回答相关问题:
现有一种不纯的氧化铁粉末样品(杂质为铁粉),小刚和小强通过实验测定样品中氧化铁的质量分数.请你回答相关问题:
(1)小刚称取10g样品,利用下图所示装置进行实验,相关实验数据见下表:(玻璃管内的物质完全反应)
| 编号 | 称量物 | 反应前 | 反应后 |
| 一 | 硬质玻璃管及所盛固体总质量 | 76.2g | 73.8g |
| 二 | B装置总质量 | 153.7g | 160.3g |
②请根据B装置总质量变化的数据,计算出样品中氧化铁的质量分数(写出计算过程).
解:设样品中氧化铁的质量为x.
(2)为达到同样的实验目的,小强设计的方案为:将一定质量的样品于过量的稀盐酸反应,准确称量反应前、后固体和液体物质的总质量,据此可求出氧化铁的质量分数.
请你分别对小刚和小强设计的实验方案进行评价(各写出一条即可):______.
(3)如果小强还想计算出所用稀盐酸的溶质质量分数,请简要说明对其方案的改进方法及原因:______;
______.
现有一种不纯的氧化铁粉末样品(杂质为铁粉),小刚和小强通过实验测定样品中氧化铁的质量分数。请你回答相关问题:
⑴小刚称取10g样品,利用下图所示装置进行实验,相关实验数据见下表:(玻璃管内的物质完全反应)
| 编号 | 称量物 | 反应前 | 反应后 |
| 一 | 硬质玻璃管及所盛固体总质量 | 76.2g | 73.8g |
| 二 | B装置总质量 | 153.7g | 160.3g |
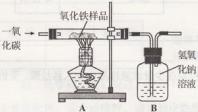
①由上表的数据可分析出,反应后硬质玻璃管及所盛固体总质量减少的是__________的质量。
②请根据B装置总质量变化的数据,计算出样品中氧化铁的质量分数(写出计算过程)。
解:设样品中氧化铁的质量为x。
⑵为达到同样的实验目的,小强设计的方案为:将一定质量的样品于过量的稀盐酸反应,准确称量反应前、后固体和液体物质的总质量,据此可求出氧化铁的质量分数。
请你分别对小刚和小强设计的实验方案进行评价(各写出一条即可):__________________________________________________________________。
⑶如果小强还想计算出所用稀盐酸的溶质质量分数,请简要说明对其方案的改进方法及原因:_________________________________________________________________;
__________________________________________________________________。
(2010?青岛)现有一种不纯的氧化铁粉末样品(杂质为铁粉),小刚和小强通过实验测定样品中氧化铁的质量分数.请你回答相关问题:
(1)小刚称取10g样品,利用下图所示装置进行实验,相关实验数据见下表:(玻璃管内的物质完全反应)
①由上表的数据可分析出,反应后硬质玻璃管及所盛固体总质量减少的是______的质量.
②请根据B装置总质量变化的数据,计算出样品中氧化铁的质量分数(写出计算过程).
解:设样品中氧化铁的质量为x.
(2)为达到同样的实验目的,小强设计的方案为:将一定质量的样品于过量的稀盐酸反应,准确称量反应前、后固体和液体物质的总质量,据此可求出氧化铁的质量分数.
请你分别对小刚和小强设计的实验方案进行评价(各写出一条即可):______.
(3)如果小强还想计算出所用稀盐酸的溶质质量分数,请简要说明对其方案的改进方法及原因:______;
______.
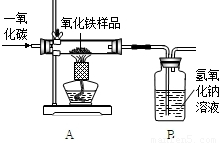
(1)小刚称取10g样品,利用下图所示装置进行实验,相关实验数据见下表:(玻璃管内的物质完全反应)
| 编号 | 称量物 | 反应前 | 反应后 |
| 一 | 硬质玻璃管及所盛固体总质量 | 76.2g | 73.8g |
| 二 | B装置总质量 | 153.7g | 160.3g |
②请根据B装置总质量变化的数据,计算出样品中氧化铁的质量分数(写出计算过程).
解:设样品中氧化铁的质量为x.
(2)为达到同样的实验目的,小强设计的方案为:将一定质量的样品于过量的稀盐酸反应,准确称量反应前、后固体和液体物质的总质量,据此可求出氧化铁的质量分数.
请你分别对小刚和小强设计的实验方案进行评价(各写出一条即可):______.
(3)如果小强还想计算出所用稀盐酸的溶质质量分数,请简要说明对其方案的改进方法及原因:______;
______.