题目内容
【题目】请写出相应的化学符号表达式
(1)有水参加的分解反应_________
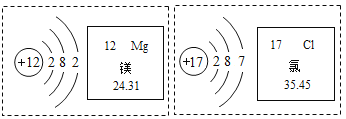
(2)一种物质与氧气反应放出耀眼的白光,可做照明弹_________
(3)在空气中不能燃烧,在纯氧中却剧烈燃烧,火星四射,并生成黑色固体物质_________
(4)有水生成的分解反应_________
【答案】H2O![]() H2+O2 Mg+O2
H2+O2 Mg+O2![]() MgO Fe+O2
MgO Fe+O2![]() Fe3O4 H2O2
Fe3O4 H2O2![]() H2O+O2
H2O+O2
【解析】
(1)分解反应是一变多的反应,水必须是反应物,所以水分解生成氧气和氢气的反应就满足要求,故答案为:H2O![]() H2+O2.
H2+O2.
(2)镁在氧气中燃烧时发出耀眼的白光,可做照明弹,反应的化学符号表达式为:Mg+O2![]() MgO;
MgO;
(3)铁在氧气中燃烧火星四射,生成四氧化三铁,反应的化学符号表达式为:Fe+O2![]() Fe3O4;
Fe3O4;
(4)分解反应是一变多的反应,生成物中必须有水,所以过氧化氢分解成水和氧气的反应就满足要求,故答案为:H2O2![]() H2O+O2。
H2O+O2。

【题目】某兴趣小组在制取氧气的实验过程中,有如下实验设计方案,该方案的实验目的是:探究氯酸钾和二氧化锰的质量比对反应速率的影响。
编号 | 温度 | 催化剂 | 氯酸钾、二氧化锰的质量比 | 生成1升氧气所需时间/s |
实验Ⅰ | 400℃ | MnO2 | 1:1 | 153 |
实验Ⅱ | 400℃ | MnO2 | 2:1 | 240 |
小芳在实验时,误把氧化铜当作二氧化锰放入加热,结果发现也能较快产生氧气,于是进行如下探究:
猜想Ⅰ:除二氧化锰、氧化铜外,氧化铁(Fe2O3)也可以作氯酸钾分解的催化剂。
(设计实验)按下表进行实验,并测定开始产生气体时的温度(提示:开始产生气体的温度越低,表示反应速度越快)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾和二氧化锰(质量比1︰1) | 350 |
③ | 氯酸钾和氧化铜(质量比1︰1) | 370 |
④ | 氯酸钾和氧化铁(质量比1︰1) | 390 |
(数据和结论)
(1)由实验_______与实验④对比,证明猜想合理;
(2)实验所用的三种物质中,催化效果最好的是_______。
(反思)
若要证明氧化铁是该反应的催化剂,还需验证它在化学反应前后的________和_______是否改变。
猜想Ⅱ:过氧化钙与水反应可制取氧气。
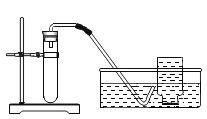
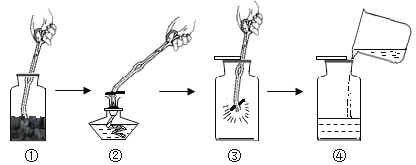
实验装置 | 实验主要过程 |
| ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。 |
实验结论:过氧化钙与水反应可制取氧气。
(分析与反思)
同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气
你认为猜想______(填序号)一定是错误的,理由是________,过氧化钙与水反应虽然没有快速收集到大量氧气,但过氧化钙在水中持续、缓慢放出氧气,因此小林认为渔民用过氧化钙做增氧剂。写出此反应的符号表达式________。
(计算)
该兴趣小组的同学们购得用于增氧的过氧化钙产品(杂质不含钙元素),标签如图所示。试计算:

(1)过氧化钙的相对分子质量为_______
(2)该产品中过氧化钙的质量分数至少为______。
(3)小组同学将3g某物质在制得的足量氧气中充分燃烧生成4.4g二氧化碳和1.8g水,求该物质中各元素的原子个数比(写出计算过程)。______