题目内容
【题目】小明家的下水管道堵塞了,他从超市购买了一种名为“管道通”的药剂,打开包装后发现里面有灰色粉末和白色粉末各一袋,商品的部分标签如图1所示:

为了弄清这种“管道通”的化学成分和工作原理,小明进行了如下实验探究:
实验一:鉴别A、B粉末的成分,请你将下表补充完整。
实验操作 | 实验现象 | 实验结论 |
取少量灰色粉末于试管中,加入适量水, 振荡,用手触摸试管外壁 | 灰色粉末不溶解, 无明显现象 | 灰色粉末是铝粉 |
取少量白色粉末于试管中,加入适量水, 振荡,用手触摸试管外壁 | 白色粉末溶解, __________________ | 白色粉末是氢氧化钠 |
实验二:探究管道疏通的原理
【查阅资料】(1)下水管道里的淤积物主要为油污、食物残渣、毛发等;
(2)氢氧化钠是强碱,能去除油污、腐蚀毛发一类的东西,常用于疏通管道;
(3)铝能与氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和氢气,同时放出大量的热。偏铝酸钠(NaAlO2)是一种盐,易溶于水,溶液显碱性。写出铝与氢氧化钠溶液反应的化学方程式:______________。
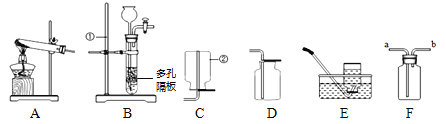
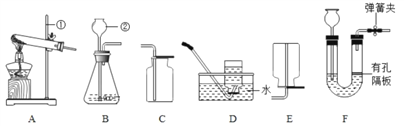
【进行实验】小明用如图2示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说明依次加入铝粉、氢氧化钠和水,并用胶塞堵住弯管上口,观察到的现象是___________________,堵塞物体变软,落入废液杯中。
【交流拓展】为了确认实验二中的废液里否有氢氧化钠剩余,小明取少量废液于试管中,滴加几滴酚酞溶液,溶液变红,于是他得出结论:废液中有氢氧化钠剩余。你认为该结论______________(填“正确”或“不正确”),理由是____________________________。
【答案】 试管外壁发烫 2Al+2NaOH+2H2O ![]() 2NaAlO2+3H2↑ 弯管外壁发烫(或弯管内的温度明显升高)、产生大量气泡 不正确 偏铝酸钠溶液显碱性,也能使酚酞溶液变红
2NaAlO2+3H2↑ 弯管外壁发烫(或弯管内的温度明显升高)、产生大量气泡 不正确 偏铝酸钠溶液显碱性,也能使酚酞溶液变红
【解析】实验一:实验过程如下表所示:
操作 | 现象 | 结论 |
取少量灰色粉末于试管中,加入适量水, 振荡,用手触摸试管外壁 | 粉末不溶解,无明显现象 | 灰色粉末是铝粉 |
取少量白色粉末于试管中,加入适量水, 振荡,用手触摸试管外壁 | 粉末溶解,试管外壁发烫 | 白色粉末是氢氧化钠 |
实验二:(3)根据质量守恒定律可知,铝与氢氧化钠溶液反应的化学方程式是:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;【进行试验】小明用如图2示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说明依次加入铝粉、氢氧化钠和水,并用胶塞堵住弯管上口,观察到的现象是弯管内的温度明显升高,产生大量气体,堵塞物体变软被气体赶出,落入废液杯中;【交流拓展】这种方法不正确,理由是偏铝酸钠溶液显碱性,能使酚酞试液变红色。

 一线名师提优试卷系列答案
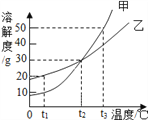
一线名师提优试卷系列答案【题目】图表法是一种常用的数据处理方法,根据所给图表(氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示),下列说法正确的是( )
氢氧化钠 | 碳酸钠 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |

A. 上述图象表示碳酸钠的溶解度曲线
B. 20℃时,氢氧化钠的溶解度大于碳酸钠
C. 40℃时,若将 50g NaOH 分别投入到 100g 水和 100g 酒精中,都能形成饱和溶液
D. 40℃时,将适量 CO2 通入饱和的 NaOH 酒精溶液中,观察不到明显的现象