��Ŀ����
(4��)���ж���ɽ��ʢ��ʯ��ʯ,ijУ����С��Ϊ�˽�ʯ��ʯ��Դ��Ʒ��,�������ַ����Ե���ʯ�Ľ��л�ѧ����:
����һ: ȡ10gʯ��ʯ��ĩ��Ʒ������ͼ��ʾװ��,��ּ����������㶨,��ȴ��Ƶù�������Ϊ8.12g
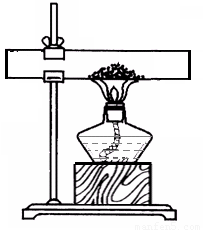
������:��ȡ10gͬ�ʵ�ʯ��ʯ������Ʒ,�����ձ��м�����ϡ����,��ַ�Ӧ��Ƶû�����������������4.27g
�������:
����ʯ��ʯ���е���Ҫ�Ӽ�Ϊ��������,�仯ѧ�����ȶ�,���Ȳ��ֽ��Ҳ������ᷢ����ѧ��Ӧ.
��������ַ�����õ�ʯ��ʯ��̼��Ƶ���������:
(1)����һ��̼��Ƶ����������� ;
(2)��������̼��Ƶ����������� .(��ȷ��0.1%)
�Ƚ������������Ľ��,�������������ϴ�Ŀ���ԭ��?
��1�����ɶ�����̼������Ϊ10g��8.12g=1.88g��������1.88g������̼��̼��Ƶ�����Ϊx��
CaCO3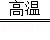 CaO+CO2��
CaO+CO2��
100 44
x 1.88g
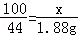
x=4.27g
ʯ��ʯ��Ʒ��̼��Ƶ����������� ��100%=42.7%��
��100%=42.7%��
��2��������������������4.27g˵��������4.27g������̼������Ʒ�е�̼��Ƶ�����Ϊy��
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
y 4.27g
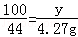
y=9.7g
ʯ��ʯ��Ʒ��̼��Ƶ�����������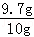 ��100%=97%��
��100%=97%��
ʯ��ʯ�ֽ���Ҫ���£����������ϴ��ԭ������Ǿƾ��ƻ����¶�ƫ�ͣ�ʯ��ʯ��ĩδ�ܳ�ַֽ⣬�������ϴ�
��������������Ҫ����ѧ������ȫ��Ӧ�ĸ�������⣬�Լ����û�ѧ����ʽ������������ʽ���м�������������ݻ�ѧ����ʽ����ʱһ��Ҫע���ʽ�ͼ����ȷ�ԣ���1��̼������ȷֽ����������ƺͶ�����̼��������ٵ������������ɶ�����̼�����������ݻ�ѧ����ʽ��ͨ��������̼�����������̼��Ƶ�������Ȼ�����ʯ��ʯ��̼��Ƶ�������������2��̼��ƺ����ᷴӦ���ɶ�����̼���壬��Ӧ����������������ٵ������������ɶ�����̼�����������ݶ�����̼�ɼ���̼��Ƶ���������������̼��Ƶ�������������̼��Ʒֽ���Ҫ���·������ַ��������ԭ��

 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�