题目内容
有四瓶失去标签的溶液:硝酸钡、碳酸钠、稀硫酸、盐酸.为了鉴别它们做了如下实验:①A和B混合有无色气体放出;②D和B混合有无色气体放出;③C和A混合没有明显现象.
根据现象推断A、B、C、D分别是什么物质,写出它们的名称和有关的化学方程式.
(1)则A是 B是 C是 D是 .
(2)D+B的反应方程式
(3)C+D的反应方程式 .
根据现象推断A、B、C、D分别是什么物质,写出它们的名称和有关的化学方程式.
(1)则A是
(2)D+B的反应方程式
(3)C+D的反应方程式
考点:酸、碱、盐的鉴别,书写化学方程式、文字表达式、电离方程式
专题:物质的鉴别题
分析:根据题意,四瓶失去标签的溶液:硝酸钡、碳酸钠、稀硫酸、盐酸,A和B混合有无色气体放出,D和B混合有无色气体放出,C和A混合没有明显现象,结合碳酸钠与稀硫酸、盐酸反应生成二氧化碳气体,则B为碳酸钠溶液;A和D为稀硫酸、稀盐酸,则C为硝酸钡;由于C和A混合没有明显现象,而硝酸钡与稀硫酸反应生成硫酸钡白色沉淀,与稀盐酸不反应,据此进行分析解答.
解答:解:(1)四瓶失去标签的溶液:硝酸钡、碳酸钠、稀硫酸、盐酸,A和B混合有无色气体放出,D和B混合有无色气体放出,C和A混合没有明显现象,碳酸钠与稀硫酸、盐酸反应生成二氧化碳气体,则B为碳酸钠溶液;A和D为稀硫酸、稀盐酸,则C为硝酸钡;由于C和A混合没有明显现象,而硝酸钡与稀硫酸反应生成硫酸钡白色沉淀,与稀盐酸不反应,故A为稀盐酸,D为稀硫酸.
(2)D+B反应生成硫酸钠、水和二氧化碳,反应的化学方程式为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
(3)C+D反应生成硫酸钡沉淀和硝酸,反应的化学方程式为:H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
故答案为:(1)盐酸;碳酸钠;硝酸钡;稀硫酸;
(2)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
(3)H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
(2)D+B反应生成硫酸钠、水和二氧化碳,反应的化学方程式为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
(3)C+D反应生成硫酸钡沉淀和硝酸,反应的化学方程式为:H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
故答案为:(1)盐酸;碳酸钠;硝酸钡;稀硫酸;
(2)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
(3)H2SO4+Ba(NO3)2═BaSO4↓+2HNO3.
点评:本题有一定难度,解答不另加试剂就能鉴别的题目时,若都没有颜色,可将溶液两两混合,根据混合后的现象进行鉴别.

练习册系列答案
相关题目
某同学给试管里的固体加热,实验结束后发现试管已破裂,请分析造成破裂的原因不可能是( )
| A、没有预热试管 |
| B、清洗试管后外壁没有擦干 |
| C、试管口没有略向下倾斜 |
| D、加入的固体药品太多 |
保持氢气化学性质的粒子是( )
| A、2H | ||
B、
| ||
| C、H2 | ||
| D、H+ |
 ”表示A原子,“
”表示A原子,“ ”表示B原子,“
”表示B原子,“ ”表示C原子,在点燃条件下,每四个甲分子能与三个乙分子反应,生成两个丙分子和六个丁分子.从微观角度回答下列问题:
”表示C原子,在点燃条件下,每四个甲分子能与三个乙分子反应,生成两个丙分子和六个丁分子.从微观角度回答下列问题: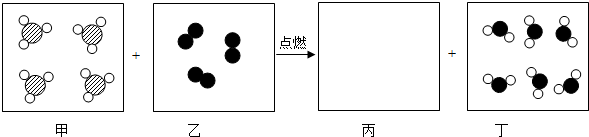
 化学与人类生活息息相关.
化学与人类生活息息相关.