题目内容
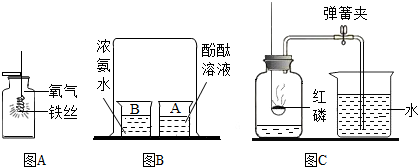
32、化学是以实验为基础的自然科学,通过实验现象的观察和分析得到结论.结合下列实验回答问题.
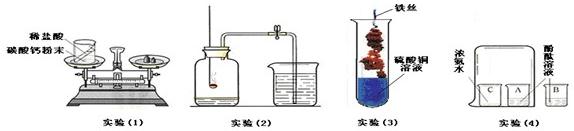
(1)实验(1)测得反应前后物质的质量
(2)实验(2)用于测定空气中氧气的含量,连接好仪器后要进行的操作是
(3)实验(3)观察到的现象是
(4)实验(4)中B烧杯用于做对比,对比得出的结论是

(1)实验(1)测得反应前后物质的质量
变小
(填“相等”“变大”或“变小”).(2)实验(2)用于测定空气中氧气的含量,连接好仪器后要进行的操作是
检查装置的气密性
,通过该实验得出的结论是
空气中氧气约占空气总体积的五分之一
.(3)实验(3)观察到的现象是
铁丝表面有红色物质生成,溶液由蓝色逐渐变为浅绿色
,该反应的化学方程式为
Fe+CuSO4=Cu+FeSO4
.(4)实验(4)中B烧杯用于做对比,对比得出的结论是
空气不能使无色酚酞试液变色
.分析:(1)在验证质量守恒定律时,若有气体参加或生成的实验必须在密闭的环境中进行.
(2)有气体参加或有气体生成的反应装置气密性应当良好,红磷消耗了空气中的氧气.
(3)铁与硫酸铜反应置换出了硫酸铜中的铜,生成了硫酸亚铁.
(4)A烧杯没与空气接触,B烧杯与空气接触,实际上是进行对比.
(2)有气体参加或有气体生成的反应装置气密性应当良好,红磷消耗了空气中的氧气.
(3)铁与硫酸铜反应置换出了硫酸铜中的铜,生成了硫酸亚铁.
(4)A烧杯没与空气接触,B烧杯与空气接触,实际上是进行对比.
解答:解:(1)碳酸钙与盐酸反应生成了二氧化碳气体,又没在密闭容器中,会逸到空气中,导致生成物质量减小,故答案为:变小.
(2)该反应是用红磷消耗氧气而验证空气中的氧气含量,需要密闭性较好的容器,故答案为:检查装置的气密性,空气中氧气约占空气总体积的五分之一.
(3)本题的反应是铁与硫酸铜反应生成了硫酸亚铁和铜,溶液的颜色由蓝色变成了浅绿色,铜在铁表面析出,故答案为:铁丝表面有红色物质生成,溶液由蓝色逐渐变为浅绿色,Fe+CuSO4=Cu+FeSO4.
(4)A被罩在烧杯中,B在空气中与空气接触,形成了对比,故答案为:空气不能使无色酚酞试液变色.
(2)该反应是用红磷消耗氧气而验证空气中的氧气含量,需要密闭性较好的容器,故答案为:检查装置的气密性,空气中氧气约占空气总体积的五分之一.
(3)本题的反应是铁与硫酸铜反应生成了硫酸亚铁和铜,溶液的颜色由蓝色变成了浅绿色,铜在铁表面析出,故答案为:铁丝表面有红色物质生成,溶液由蓝色逐渐变为浅绿色,Fe+CuSO4=Cu+FeSO4.
(4)A被罩在烧杯中,B在空气中与空气接触,形成了对比,故答案为:空气不能使无色酚酞试液变色.
点评:有气体参与的反应在涉及质量时要在密闭性好的容器中进行反应,识记性较强.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目