题目内容
【题目】下面是实验老师在实验室用双氧水和二氧化锰制取氧气的装置图: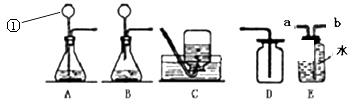
请回答:
(1)写出标号①仪器的名称;
(2)该老师制取氧气应选用的发生装置是(填字母编号);写出该方法制取氧气的化学反应方程式;收集氧气可选用D装置。理由是;如果用E装置收集氧气,则气体应从(填“a”或“b”)进入。
(3)上面发生装置还可以用于实验室制取其他气体,请写出制取其中一种气体化学方程式:。
【答案】
(1)长颈漏斗
(2)A,2H2O2![]() 2H2O + O2↑,氧气的密度大于空气,a
2H2O + O2↑,氧气的密度大于空气,a
(3)Zn + H2SO4 = ZnSO4 + H2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑
【解析】(1)由仪器的图形和用途可知①为长颈漏斗;
(2)过氧化氢溶液在二氧化锰催化作用下生成水和氧气,二氧化锰在反应前后质量和化学性质都没有改变,只是加快了过氧化氢反应生成氧气的速率,故二氧化锰是催化剂,所以二氧化锰就应该作为反应条件写在等号的上方,故化学方程式为:2H2O2![]() 2H2O+O2↑,由于反应不需要加热,所以发生装置可选A(B装置中长颈漏斗下端没有伸入液面以下,会导致产生的氧气顺着长颈漏斗跑掉);由于氧气密度比空气大,所以可用向上排空气法收集;
2H2O+O2↑,由于反应不需要加热,所以发生装置可选A(B装置中长颈漏斗下端没有伸入液面以下,会导致产生的氧气顺着长颈漏斗跑掉);由于氧气密度比空气大,所以可用向上排空气法收集;
由于E装置内装满水,如果氧气从b管进入集气瓶,由于氧气的密度远小于水的密度,进入集气瓶内的氧气会从a管中导出;而从a管进入,由于氧气不易溶于水,在氧气压力的不断增大下,集气瓶中的水会被压出,当水被排净时,集气瓶内就充满氧气.
(3)A装置的特点是固体和液体反应且不需加热,实验室用锌和稀硫酸制取氢气、石灰石和稀盐酸制取二氧化碳都是固体和液体反应且不需加热,所以都可用上面的A装置来制取.其中锌和稀硫酸反应生成氢气的同时还生成硫酸锌,所以其化学方程式为:Zn+H2SO4=ZnSO4+H2↑;石灰石和稀盐酸反应生成氯化钙、水和二氧化碳,所以其反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
故答案为:(1)长颈漏斗;(2)A; 2H2O2![]() 2H2O+O2↑;氧气的密度大于空气;a;(3)Zn+H2SO4=ZnSO4+H2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑.
2H2O+O2↑;氧气的密度大于空气;a;(3)Zn+H2SO4=ZnSO4+H2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑.
(1)根据常用仪器的名称解答即可;
(2)用过氧化氢和二氧化锰制氧气时,过氧化氢在二氧化锰催化作用下生成水和氧气;根据反应物的状态和反应条件可选择发生装置,根据氧气的密度以及溶于水的程度可选择收集装置;如果用E装置收集氧气,导管要短进长出;
(3)实验室用锌和稀硫酸制取氢气、石灰石和稀盐酸制取二氧化碳都可以用A装置来制取,锌和稀硫酸反应生成氢气的同时还生成硫酸锌,的同时还生成硫酸锌,石灰石和稀盐酸反应生成氯化钙、水和二氧化碳.