题目内容
【题目】工业上用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙).主要流程如图所示: 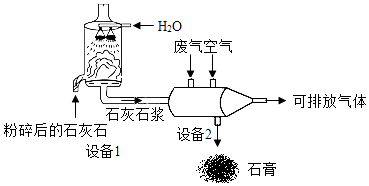
(1)设备1中,石灰石加水制成石灰石浆的目的是 . 设备2中的主要反应为:2CaCO3+2SO2+O2═2CaSO4+2X,则X的化学式为 .
(2)按上述方法处理2000t废气中的二氧化硫,至少需要含5t碳酸钙的石灰石浆.计算废气中二氧化硫的质量为t.
【答案】
(1)增大反应物的接触面积,使石灰石与二氧化硫充分反应;CO2
(2)3.2
【解析】解:(1)设备1中,石灰石加水制成石灰石浆的目的是增大反应物的接触面积,使石灰石与二氧化硫充分反应;
由2CaCO3+2SO2+O2═2CaSO4+2X可知,反应前后钙原子、硫原子的个数都是2个,反应前碳原子是2个,反应后应该是2个,包含在2X中,反应前氧原子个数是12个,反应后应该是12个,其中4个包含在2X中,则X的化学式为CO2.
故填:增大反应物的接触面积,使石灰石与二氧化硫充分反应;CO2.(2)设废气中二氧化硫的质量为x,
2CaCO3+ | 2SO2+O2═2CaSO4+2CO2 |
200 | 128 |
5t | x |
![]() =
= ![]() ,
,
x=3.2t,
故填:3.2.
反应物接触越充分,反应速率越快;
化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类和总个数不变;
根据反应的化学方程式和碳酸钙的质量可以计算二氧化硫的质量.

【题目】纳米级铁粉常用作食品脱氧剂,但该铁粉在空气中易自燃,需小心保存. 某课外小组同学经查阅资料,在实验室设计实验并制取食品脱氧剂,流程如图所示.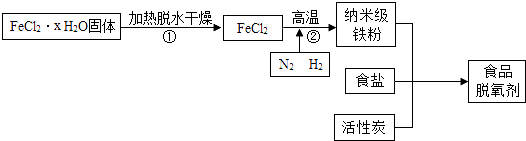
(1)①食品脱氧剂属于(填“纯净物”或“混合物”). ②过程②中,H2与FeCl2在高温下发生的是置换反应,请写出该反应的化学方程式 .
③过程②中氮气不参与反应,通入N2的目的是 .
(2)合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出来巨大贡献.合成氨工艺的主要流程如下: 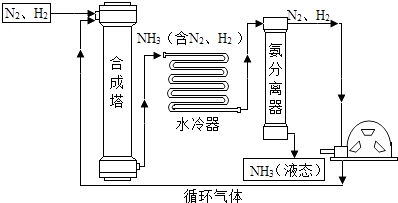
①合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是 .
②生产过程中可循环使用的物质是 .
③根据表中的数据回答问题.
物质 | H2 | N2 | O2 | NH3 |
沸点/℃(1.01×105Pa) | ﹣252 | ﹣195.8 | ﹣183 | ﹣33.35 |
在1.01×105Pa时,欲将NH3与N2、H2分离,适宜的方法是 .