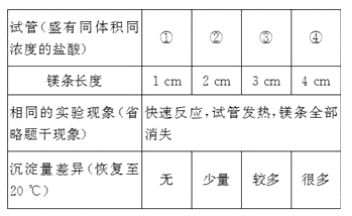
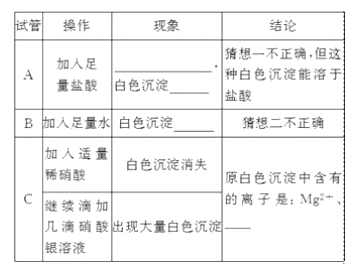
��Ŀ����
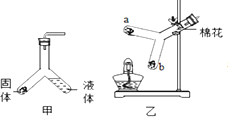
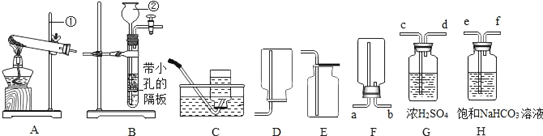
����Ŀ����ѧ�����ס�Ÿ������ʡ���������������Ϊ�ػ�����ʿ�����ֱ����������ᡢ����ͭ������������̼���ơ�ֻ���������ʼ��ܷ�����Ӧ��������ػ��ķ��ߣ���ͼ��ʾ������������B������θҺ�е���Ҫ�ɷ����ʣ�����E���ڼ��ࡣ
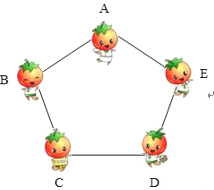
��1��A���ʵ�ˮ��Һ�м�����ɫʯ���Һ��_____ɫ��E���ʵĻ�ѧʽ��_____
��2��A��B�ķ�Ӧ����_____��Ӧ���������Ӧ���ͣ���C��D��Ӧʱ��ʵ������Ϊ_____��
��3����������������Ϊ����С��ֱ��Χ�ݷ��������������������λ���ڵ��ػ�����ʿ�����ܷ�����Ӧ���ܹ��Ʒ��ߣ���ô�ܹ���Χ�ݵ�������_____������ţ���д�������Ļ�ѧ��Ӧ����ʽ_____����д����һ�����ɣ�
��������̼�������������������������ᡡ���������������ơ�
���𰸡��� Ba��OH��2 ���ֽ� ��˿�����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ �� Ba��OH��2+H2SO4��BaSO4��+2H2O
��������
���ݡ�����B������θҺ�е���Ҫ�ɷ����ʡ������Ʋ�BΪϡ������ݡ�����E���ڼ��ࡱ�����Ʋ�EΪ������������Ϊ����ϡ���ᷴӦ����������ͭ��Һ��Ӧ������������Һ������ͭ��Һ��Ӧ������������Һ��̼������Һ��Ӧ��̼������ϡ���ᷴӦ�����Ʋ�AΪ̼������Һ��CΪ����DΪ����ͭ��Һ��������飻
��1�����ݷ�����A����Ϊ̼���ƣ���ˮ��ҺΪ���ԣ��ʼ�����ɫʯ���Һ����ɫ��
���ݷ�����EΪ������������E���ʵĻ�ѧʽ��Ba��OH��2��
��2��A��B�ķ�Ӧ����ϡ������̼������Һ��Ӧ�����Ȼ��ƺ�ˮ��������̼�����ڸ��ֽⷴӦ��C��D��Ӧ������������ͭ��Һ��Ӧ����Ӧ��ʵ������Ϊ����˿�����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ��
��3����Ϊ������ֻ̼��������������Һ��Ӧ��������ֻ��ϡ���ᷴӦ��������̼���ƺ�������������Ӧ����������ֻ������ͭ��Һ��Ӧ����������������λ���ڵ��ػ�����ʿ�����ܷ�����Ӧ���ܹ��Ʒ��ߣ���ô�ܹ���Χ�ݵ�������ϡ���ᣬ��ѡ���������Ļ�ѧ��Ӧ����ʽ Ba��OH��2+H2SO4��BaSO4��+2H2O��Na2CO3+H2SO4��Na2SO4+H2O+CO2��������д����һ�����ɣ�
�ʴ�Ϊ��
��1������Ba��OH��2����2�����ֽ⣻ ��˿�����к�ɫ������֣���Һ����ɫ��Ϊdz��ɫ����3������Ba��OH��2+H2SO4��BaSO4��+2H2O��