题目内容
【题目】如图所示,在白色点滴板1﹣6的孔穴中,分别滴加2滴紫色石蕊溶液. 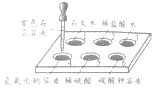
(1)孔穴6中溶液变为蓝色,说明碳酸钾溶液显(填“酸性”或“碱性”).
(2)溶液变为红色的孔穴有(填孔穴序号,下同).
(3)作为空白对照实验的孔穴是
(4)再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因:
【答案】
(1)碱性
(2)2、5
(3)3
(4)2NaOH+H2SO4=Na2SO4+2H2O
【解析】解:(1)紫色石蕊遇碱性物质变蓝,孔穴6中溶液变为蓝色,说明碳酸钾溶液显碱性.(2)紫色石蕊遇酸性物质变红,1石灰水显碱性,2稀盐酸显酸性,3水为中性,4氢氧化钠溶液显碱性,5稀硫酸显酸性,6碳酸钾溶液显碱性.(3)3水为中性,紫色石蕊不变色,起对照作用;(4)孔穴4中原来是氢氧化钠,向其中滴加稀硫酸,发生中和反应,方程式为2NaOH+H2SO4=Na2SO4+2H2O.但恰好反应时,溶液显中性,溶液变为紫色. 所以答案是:(1)碱性;(2)2,5;(3)3;(4)2NaOH+H2SO4=Na2SO4+2H2O.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号才能正确解答此题.

练习册系列答案
相关题目
【题目】除去物质中的少量杂质,下列方法不能达到目的的是( )
选项 | 物质 | 杂质 | 除去杂质的方法 |
A | CaO | CaCO3 | 高温充分煅烧 |
B | KCl溶液 | CaCl2 | 通入足量的CO2 , 过滤 |
C | CO2 | CO | 通过足量的灼热氧化铜 |
D | H2 | HCl | 依次通过足量的NaOH溶液和浓硫酸 |
A.A
B.B
C.C
D.D