题目内容
【题目】人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色。
(1)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属_____的位置移到最后,正好符合由弱到强的顺序。
(2)汽车车体多用钢材制造。表面_____不仅美观,而且可有效防止生锈。
(3)工业冶炼金属:
①工业上用CO还原赤铁矿冶炼金属铁的化学方程式为_____。工业冶铁的原料有石灰石、铁矿石、空气及焦炭,其中焦炭的作用有_____、_____;石灰石首先在高温下发生分解,其化学反应方程式为_____;其分解产物与铁矿石的杂质结合成炉渣。
②中国古老的冶铜方法“湿法冶铜”主要的反应原理是_____(写化学方程式)。
(4)在实验室中探究铝、铜、银的金属活动性顺序,除铝、银外,还需要用到的试剂是_____。(填化学式)
(5)铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图。

①使用铁锅是利用金属的_____,
②家庭用的燃料大多为天然气,写出天然气燃烧的化学方程式_____。炒菜时铁锅中的油着火可用锅盖盖灭,其原理是_____。
③铜也易生锈,铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],是铜与空气中的_____共同作用的结果。
【答案】铁 喷漆 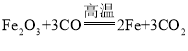 作还原剂 提供热量
作还原剂 提供热量 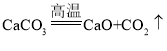
![]()
![]() 导热性
导热性 ![]() 隔绝空气 水蒸气、氧气、二氧化碳
隔绝空气 水蒸气、氧气、二氧化碳
【解析】
(1)由金属活动性顺序表可知,在“五金”顺序中把金属铁的位置移到最后,正好符合由弱到强的金属活动性顺序。
(2)汽车车体多用钢材制造,钢铁与氧气、水接触容易生锈,表面喷漆不仅美观,而且可有效防止生锈。
(3)①工业上用CO还原赤铁矿冶炼金属铁的原理是,高温条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为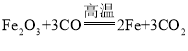 。工业冶铁的原料有石灰石、铁矿石、空气及焦炭,其中焦炭具有还原性,燃烧放出大量的热,作用有作还原剂、提供热量;石灰石首先在高温下发生分解,生成氧化钙和二氧化碳,其化学反应方程式为
。工业冶铁的原料有石灰石、铁矿石、空气及焦炭,其中焦炭具有还原性,燃烧放出大量的热,作用有作还原剂、提供热量;石灰石首先在高温下发生分解,生成氧化钙和二氧化碳,其化学反应方程式为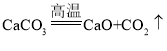 。
。
②“湿法冶铜”主要的反应原理是铁与硫酸铜溶液反应,反应的化学方程式是:![]() 。
。
(4)在实验室中探究铝、铜、银的金属活动性顺序,除铝、银外,还需要用到的试剂是硫酸铜,铝能置换出铜,而银不能;故填:![]() 。
。
(5)①使用铁锅是利用金属的导热性;
②家庭用的燃料大多为天然气,天然气主要成分为![]() ,燃烧生成水和二氧化碳,反应的化学方程式为
,燃烧生成水和二氧化碳,反应的化学方程式为![]() 。炒菜时铁锅中的油着火可用锅盖盖灭,其原理是隔绝空气。
。炒菜时铁锅中的油着火可用锅盖盖灭,其原理是隔绝空气。
③根据铜锈的主要成分是碱式碳酸铜![]() ,其中铜元素化合价为+2,说明铜单质被氧化,结合质量守恒定律,铜生锈是铜与空气中的水蒸气、氧气、二氧化碳共同作用的结果。
,其中铜元素化合价为+2,说明铜单质被氧化,结合质量守恒定律,铜生锈是铜与空气中的水蒸气、氧气、二氧化碳共同作用的结果。