题目内容
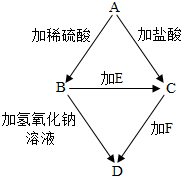 在复习时,小英归纳了一个有关元素化合物的知识网络(如图).其中A、B、C、D是四种不同的含铁化合物,A为铁锈的主要成分,E、F为两中无色溶液.根据网络图进行判断:
在复习时,小英归纳了一个有关元素化合物的知识网络(如图).其中A、B、C、D是四种不同的含铁化合物,A为铁锈的主要成分,E、F为两中无色溶液.根据网络图进行判断:(1)写出E、F中溶质的化学式
E
(2)用化学方程式表示下列变化
A→C
分析:根据A是铁锈的主要成分,因此A是氧化铁;A、B、C、D是四种不同的含铁化合物,因此B是氧化铁和稀硫酸反应产生的硫酸铁,C是氧化铁和稀盐酸反应产生的氯化铁,D是硫酸铁和氢氧化钠反应产生的氢氧化铁沉淀完成相关的问题.
解答:解:A是铁锈的主要成分,因此A是氧化铁;A、B、C、D是四种不同的含铁化合物,因此B是氧化铁和稀硫酸反应产生的硫酸铁,C是氧化铁和稀盐酸反应产生的氯化铁,D是硫酸铁和氢氧化钠反应产生的氢氧化铁沉淀,因此:
(1)因为B是硫酸铁,C是氯化铁,根据复分解反应的发生条件,Fe2(SO4)3→FeCl3,必须产生沉淀,因此加入的E是氯化钡;FeCl3→Fe(OH)3↓,必须加入可溶性的碱,如氢氧化钾等,因此E是BaCl2;F是 KOH(或NaOH等);
(2)A→C是盐酸和氧化铁的反应,因此反应的方程式为:6HCl+Fe2O3=2FeCl3+3H2O;
B→D是硫酸铁和氢氧化钠的反应,因此反应的方程式为:Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4.
故答案为:(1)BaCl2; KOH(或NaOH等);
(2)6HCl+Fe2O3=2FeCl3+3H2O; Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4.
(1)因为B是硫酸铁,C是氯化铁,根据复分解反应的发生条件,Fe2(SO4)3→FeCl3,必须产生沉淀,因此加入的E是氯化钡;FeCl3→Fe(OH)3↓,必须加入可溶性的碱,如氢氧化钾等,因此E是BaCl2;F是 KOH(或NaOH等);
(2)A→C是盐酸和氧化铁的反应,因此反应的方程式为:6HCl+Fe2O3=2FeCl3+3H2O;
B→D是硫酸铁和氢氧化钠的反应,因此反应的方程式为:Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4.
故答案为:(1)BaCl2; KOH(或NaOH等);
(2)6HCl+Fe2O3=2FeCl3+3H2O; Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4.
点评:本题是有关铁的转化的推断,依据题目提供的应该铁的信息及发生的反应结合复分解反应的发生条件进行推断即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
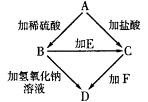


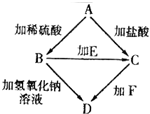 在复习时,小英归纳了一个有关元素化合物的知识网络(如图).其中A、B、C、D是四种不同的含铁化合物,A为铁锈的主要成分,E、F为两中无色溶液.根据网络图进行判断:
在复习时,小英归纳了一个有关元素化合物的知识网络(如图).其中A、B、C、D是四种不同的含铁化合物,A为铁锈的主要成分,E、F为两中无色溶液.根据网络图进行判断: