题目内容
【题目】为研究酸的性质,让研究小组的同学进行了如下探究。
(1)小涵同学将颗粒大小相同的纯锌粒和粗锌粒中分别加入相同浓度的稀硫酸中,写出锌与硫酸反应的化学方程式_______________。
(2)小涵通过观察发现纯锌粒与硫酸的反应明显比粗锌粒慢。通过查阅资料得知粗锌中含有一些不活泼金属,她猜想可能是粗锌中不活泼金属促进了锌与硫酸的反应。为了验证小涵的猜想,你认为应该在盛有纯锌粒和稀硫酸的试管中,加入下列那种物质?________,选择该物质的理由是________________。
AHCl B![]() CNaCl D
CNaCl D![]()
(3)实验中小涵发现加入上述四种物质,纯锌与稀硫酸的反应都有不同程度的加快,请你分析可能的原因是什么?__________________。
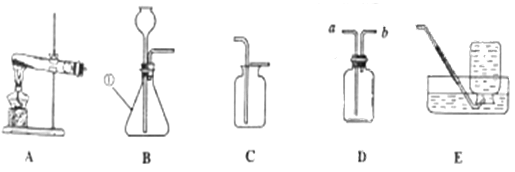
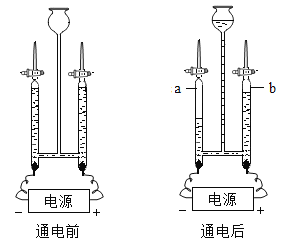
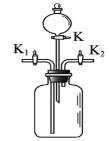
(4)小川同学想通过用一定质量粗锌与足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度,于是设计了如图所示的实验装置。
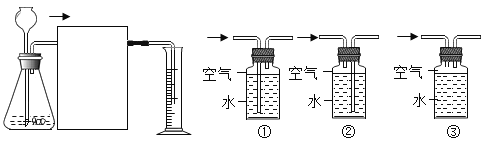
在虚线框中应接入如图中的________,广口瓶上方残留的空气________(填“会”或“不会”)对氢气体积的测量造成影响。
【答案】![]() B 锌可以置换出铜(或铜不活泼)
B 锌可以置换出铜(或铜不活泼) ![]() 加快了反应(或这些物质中都含氯元素) ② 不会
加快了反应(或这些物质中都含氯元素) ② 不会
【解析】
(1)锌粒与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
(2)由金属活动性顺序可知:钠、钙都比锌活泼,铜不如锌活泼,为了验证小涵的猜想,应该在盛有纯锌粒和稀硫酸的试管中,加入少量的CuCl2;
(3)实验中小涵发现加入上述四种物质,纯锌与稀硫酸的反应都有不同程度的加快,请你分析可能的原因是四种溶液中的Cl-对反应起了促进作用;
(4)氢气难溶于水,收集氢气时应短进长出,故用一定质量粗锌和足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度设计了如图所示的实验装置。在虚线框中应接入图中的②,因为通过排出的水来测量氢气的体积,广口瓶上方残留的空气不会对氢气体积的测量造成影响。
故答案为:
(1)Zn+H2SO4═ZnSO4+H2↑;
(2)B;在金属活动顺序中,钠、钙都比锌活泼,铜不如锌活泼;
(3)四种溶液中的Cl-对反应起了促进作用;
(4)②;不会。

 口算能手系列答案
口算能手系列答案【题目】人类的生产、生活离不开金属。
(1)铁制品在喷漆前需除锈,可用来除铁锈的物质是_____。
(2)为探究铁、铜、银三种金属的活动性顺序,设计了1、Ⅱ两种方案。
方案1 | 方案Ⅱ |
|
|
能验证三种金属活动性顺序的一种方案是_____写出发生反应的化学方程式_____。
【题目】控制变量是实验探究的重要方法,请回答下列问题:
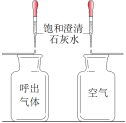
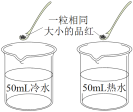
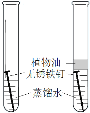
实验 编号 | 一、探究人体呼出气体中二氧化碳与空气中的含量不同 | 二、探究影响品红扩散快慢的因素 | 三、铁钉锈蚀条件的探究 |
实验 设计 |
|
|
|
实验 分析 | 本实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制_____相同。 | 发现两杯水都变红,且热水全部变红的时间比冷水短。由此说明①分子在不断运动;②影响分子运动快慢的因素有____。 | 一周后,左边试管中铁钉生锈,右边试管中铁钉无明显变化。上述实验____(填“能”或“不能”)得出铁钉生锈的条件。 |