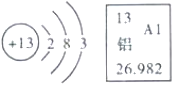
题目内容
用某矿石(主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质)制取MgO的工艺流程简图如图:
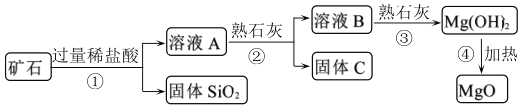
回答下列问题:
(1)步骤①和步骤②均用到的操作是_____。
(2)溶液A一定_____ (填“有”或“没有”)颜色,其中所含质量最小的阳离子是_____(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的pH范围为_____,固体C中所含成分的化学式为_____。
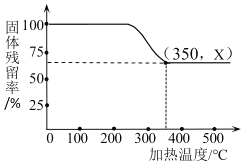
(4)已知在不同温度下,充分加热等质量的Mg(OH)2,加热温度与固体残留率的关系如图所示。则在上述流程步骤④中,加热的温度至少_____℃以 上,图中拐点的X值为_____(取整数)。
(5)写出步骤①中Fe2O3溶于盐酸的反应化学方程式:_____。
(6)上面工业流程中不用石灰水代替熟石灰工业意义是:_____(答一条即可)。
 阅读快车系列答案
阅读快车系列答案化学与人类的生活密切相关。下列对化学知识的应用归纳完全正确的一组是( )
A.化学与生活 | B.化学与安全 |
①用活性炭包可吸附汽车内的异味 ②用洗涤剂可以洗掉衣服和餐具上的油污 | ①炒菜时油锅着火可以用锅盖盖灭 ②在室内放一盆水能防止煤气中毒 |
C.化学与资源 | D.化学与健康 |
①煤、石油、天然气都是可再生能源 ②我国试采可燃冰成功,为未来使用新能源提供可能 | ①烧烤食品营养丰富,可大量食用 ②每天食用适量蔬菜,以补充维生素 |
A.A B.B C.C D.D
学习复分解反应发生条件时,小红同学做了下表中的四个实验。
试管编号 | ① | ② | ③ | ④ |
试管内试剂 | NaOH溶液 | MgCl2溶液 | Na2CO3溶液 | Ba(NO3)2溶液 |
加入硫酸后的现象 | 无明显现象 | 无明显现象 | 产生气泡 | 白色沉淀生成 |
(1)根据以上实验,可以判断试管③④中发生了复分解反应。试管③中反应的化学方程式为_________________________________。
(2)小明同学向盛有NaOH溶液的试管中先加了一种试剂,再加稀硫酸,从而能说明试管①中也发生了反应,这种试剂是___________。
(3)为了验证试管②中是否发生复分解反应,小明同学进行了如下探究。
[提出猜想]猜想1:试管②中没有发生复分解反应,溶液中有MgCl2,即Mg2+和Cl-同时存在溶液中。
猜想2:试管②中发生了复分解反应,溶液中无MgCl2。
老师提示SO42-会对Cl-的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了以下实验方案。
[设计方案]
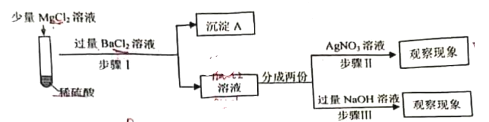
沉淀A的化学式是___________。
老师评价该方案时指出:设计思路正确,但试剂选择有误,你认为应该将所选的试剂_______改成____________。
小明按照修改后的方案进行了实验,最后得出的结论是猜想1正确,则步骤Ⅱ、步骤Ⅲ中必然会观察到的现象是____________________。
[实验反思]小明反思进行步骤Ⅲ时,加NaOH溶液采用了滴加的方式,但没有立即观察到任何现象,你认为其中的原因是_______________________。


 将饱和石灰水敞口放置在空气中一段时间
将饱和石灰水敞口放置在空气中一段时间 稀释等质量的30%的H2SO4溶液和10%的H2SO4溶液
稀释等质量的30%的H2SO4溶液和10%的H2SO4溶液 等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量
等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量 向一定量的CuSO4溶液中加入足量的铁粉
向一定量的CuSO4溶液中加入足量的铁粉