题目内容
【题目】早在春秋战国时期,我国就开始生产和使用铁器,现在,铁是世界上年产量最多的金属. 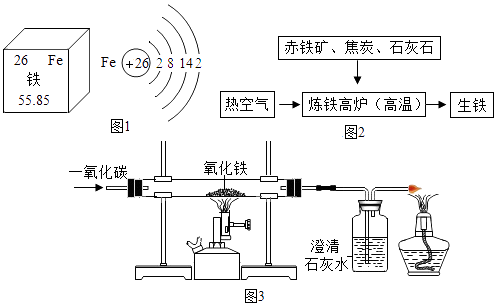
(1)如图1是元素周期表中铁元素的有关信息和铁的原子结构示意图.下列说法正确的是(填字母)
A铁在化学变化中容易得到电子
B铁元素的原子序数是26
C铁的相对原子质量是55.85g
D铁离子的符号为Fe2+
(2)如图2是工业炼铁示意图.其中,焦炭的作用是和
(3)如图3是实验室模拟工业炼铁的装置图.
①A装置硬质玻璃管里可观察到的现象是 , 所发生反应的化学方程式为 .
②B装置中可观察到的现象是 .
③C处酒精灯的作用是 .
(4)工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来.若用铝与氧化铁反应来制取22.4kg铁,理论上需要消耗铝的质量是多少?
【答案】
(1)B
(2)燃烧提供能量;制取CO
(3)红色粉末变为黑色;3CO+Fe2O3 ![]() 2Fe+3CO2;澄清石灰水变浑浊;点燃一氧化碳,防止一氧化碳污染空气
2Fe+3CO2;澄清石灰水变浑浊;点燃一氧化碳,防止一氧化碳污染空气
(4)解:设需加原料铝的质量为x
Fe2O3 | + | 2Al |
| Al2O3 | + | 2Fe |
54 | 112 | |||||
x | 22.4kg |
![]()
解得:x=10.8kg
答:需在反应中加入原料铝的质量是10.8kg
【解析】解:(1)A、铁的最外层电子数为2,所以铁在化学变化中容易失去电子,故A错误;
B、根据图中元素周期表可以获得的信息,铁元素的原子序数是26,故B正确;
C、根据图中元素周期表可以获得的信息,铁的相对原子质量是55.85,没有g,故C错误;
D铁离子的符号为Fe3+ , 故错误;
故选:B;(2)因为焦炭燃烧放出大量的热,给炼铁提供热量,同时碳燃烧生成二氧化碳,碳再与二氧化碳反应生成一氧化碳,所以制取一氧化碳,一氧化碳再作为炼铁的还原剂;故填:燃烧提供能量;制取CO;(3)①一氧化碳检验还原性,与氧化铁反应生成铁和二氧化碳,A装置硬质玻璃管里可观察到的现象是红色粉末变为黑色,反应的化学方程式为:3CO+Fe2O3 ![]() 2Fe+3CO2;故填:红色粉末变为黑色;3CO+Fe2O3
2Fe+3CO2;故填:红色粉末变为黑色;3CO+Fe2O3 ![]() 2Fe+3CO2;②二氧化碳能使澄清石灰水变浑浊,所以B装置中可观察到的现象是澄清石灰水变浑浊;故填:澄清石灰水变浑浊;③一氧化碳有毒,直接排放到空气中会造成空气污染,一氧化碳具有可燃性,燃烧生成二氧化碳,装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是点燃一氧化碳,防止一氧化碳污染空气.故填:点燃一氧化碳,防止一氧化碳污染空气;
2Fe+3CO2;②二氧化碳能使澄清石灰水变浑浊,所以B装置中可观察到的现象是澄清石灰水变浑浊;故填:澄清石灰水变浑浊;③一氧化碳有毒,直接排放到空气中会造成空气污染,一氧化碳具有可燃性,燃烧生成二氧化碳,装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是点燃一氧化碳,防止一氧化碳污染空气.故填:点燃一氧化碳,防止一氧化碳污染空气;
【考点精析】通过灵活运用一氧化碳还原氧化铁和铁的冶炼,掌握原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来;铁冶炼的原料:铁矿石、焦炭、石灰石、空气;常见的铁矿石有磁铁矿(主要成分是Fe3O4 )、赤铁矿(主要成分是Fe2O3 )即可以解答此题.

【题目】如表是KCl和KNO3在不同温度下的溶解度.请回答:
温度/℃ | 20 | 30 | 40 | 50 | |
溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
(1)20℃时,KNO3的溶解度是g.
(2)40℃时,将5gKCl加入到10g水中,充分溶解后所得溶液是(填“饱和”或“不饱和”)溶液,所得溶液中溶质的质量分数为 .