题目内容
【题目】下图所示是初中化学常见的实验装置图,请回答:
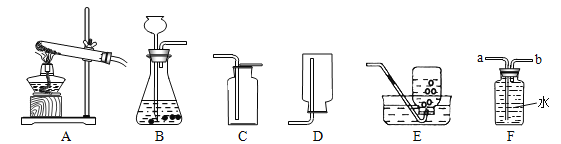
(1)实验室用B装置制取氧气,反应的化学方程式为 ;若用E装置收集的氧气不纯,则可能的原因是 (答出一种即可);若用F装置收集氧气,气体应从 (填“a”或“b”)端进入。
(2)实验室制取并收集一瓶二氧化碳气体,应选用的装置为 (填字母序号),在装入药品前应先 ,该反应的化学方程式为 。
【答案】(1)2H2O2![]() 2H2O+ O2↑ 集气瓶没装满水(或没等气泡连续均匀冒出就收集等) b
2H2O+ O2↑ 集气瓶没装满水(或没等气泡连续均匀冒出就收集等) b
(2)BC 检查装置气密性 CaCO3 + 2HCl == CaCl2 + CO2↑+ H2O
【解析】
试题分析:(1)B为固液不需加热型,因此为过氧化氢在二氧化锰催化下分解;E为排水法收集,那么不纯的原因可能是过早的收集,前期排出的为空气,或者集气瓶内原本就含有空气,即未用水将空气完全排净;氧气密度比水小,因此从b口进,水从a排出;
(2)实验室用固体石灰石和液体稀盐酸不需加热反应制取二氧化碳,因此发生装置选B,二氧化碳能溶于水,密度比空气大,因此收集装置选C;

 阅读快车系列答案
阅读快车系列答案【题目】“化学反应条件的控制是实验的灵魂”。某探究小组发现若反应过快,产生的气体不易及时收集,为探究影响过氧化氢溶液分解快慢的因素,于是进行了如下探究:
【提出问题】过氧化氢溶液分解快慢与哪些因素有关呢?
【猜想与假设】猜想一:可能与过氧化氢的质量分数有关;
猜想二:可能与 有关;
猜想三:可能与是否用催化剂有关。
【设计并实验】该探究小组用不同质量分数的过氧化氢溶液在不同温度时进行四次实验.记录所生成的氧气体积和反应所需时间,记录数据如下表.
实验 | 过氧化氢的 | 过氧化氢溶液 | 温度 | 二氧化锰 | 收集氧气 | 反应所需 |
① | 5% | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15% | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30% | 5 | 35 | 2 | 49.21 | |
④ | 30% | 5 | 55 | 2 | 10.76 |
【收集证据】要比较不同质量分数的过氧化氢溶液对反应快慢的影响,应选择的实验编号组合是
(选填“实验序号”)。由实验③和④对比可知,化学反应速率与温度的关系是: 。
【解释与结论】(1)通过探究,了解控制过氧化氢分解快慢的方法。请写出过氧化氢溶液在二氧化锰的催化作用下生成氧气的化学方程式为: 。(2)用一定量15%的过氧化氢溶液制氧气,为了减缓反应速率,可加适量的水稀释,所产生氧气的总质量 。(填“减小”、“增大”或“不变”)