题目内容
【题目】铜锈的主要成分是碱式碳酸铜.碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3 ![]() 2CuO+X+CO2↑下列说法正确的是( )
2CuO+X+CO2↑下列说法正确的是( )
A.反应前后固体物质中铜元素的质量分数不变
B.X是相对分子质量最小的氧化物
C.碱式碳酸铜原子和氧原子的个数比为2:3
D.加热Cu2(OH)2CO3的实验装置和实验室制取CO2的发生装置相同
【答案】B
【解析】解:A、由方程式可知固体质量减少,而铜元素的质量不变,因此铜元素的质量分数变大,故选项错误;B、反应前后原子的种类和个数都不变,可判断X的化学式是H2O,H2O是相对分子质量最小的氧化物,故选项正确;
C、化学式中同种原子的个数要合并,因此Cu2(OH)2CO3中铜原子和氧原子的个数比是2:5,故选项错误;
D、加热Cu2(OH)2CO3的实验装置是固体加热型的发生装置,而实验室制取二氧化碳用稀盐酸和石灰石,是固液常温型的发生装置,发生装置不同,故选项错误.
故选:B.
A、根据方程式可知固体质量减少,而铜元素的质量不变,分析元素质量分数的变化;
B、根据化学式中右下角的数字的意义分析;
C、根据反应前后原子的种类和个数都不变分析X的化学式;
D、根据反应物的状态和反应条件分析发生装置.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
【题目】某同学向如图实验装置中通入气体X,若关闭活塞A,澄清石灰水变浑浊;若打开活塞A,澄清石灰水不变浑浊,则气体X和洗气瓶内溶液Y分别可能是( ) 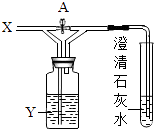
A | B | C | D | |
X | HCl | HCl | CO2 | CO2 |
Y(足量) | Na2CO3 | NaOH | 浓硫酸 | NaOH |
A.A
B.B
C.C
D.D
