题目内容
 家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢(如图).因为硬水中含有较多的可溶性的钙、镁的化合物,其中碳酸氢钙[Ca(HCO3)2],受热易分解,生成水和大量的气体,还有一种难溶性的化合物,它是水垢的成分之一.
家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢(如图).因为硬水中含有较多的可溶性的钙、镁的化合物,其中碳酸氢钙[Ca(HCO3)2],受热易分解,生成水和大量的气体,还有一种难溶性的化合物,它是水垢的成分之一.[观察与问题]碳酸氢钙受热分解的另外两种生成物质是什么?
【假设与预测】
①鸿鸿认为生成物中的固体可能是碳酸钙.
②我认为生成物中的气体可能是
[实验与事实]依据猜想我设计如下实验方案:
| 实验步骤 | 猜想正确应该的实验现象 | |
| 验证猜想①的方案 | 取少量水垢于试管,滴加稀盐酸,在试管口用燃烧着木条检验 | _________________________ ___________________________ |
| 验证猜想②的方案 | 取少量硬水于试管并加热,将生成气体通入____中 | ___________________________ |
碳酸钙与盐酸反应化学方程式:
Ca(HCO3)2受热分解的化学方程式:
分析:①碳酸钙与盐酸反应,生成氯化钙、水和二氧化碳,二氧化碳气体不能燃烧也不助燃;
②二氧化碳气体可与氢氧化钙反应,生成碳酸钙白色沉淀;
②二氧化碳气体可与氢氧化钙反应,生成碳酸钙白色沉淀;
解答:解:①因为碳酸钙与盐酸反应,生成氯化钙、水和二氧化碳,二氧化碳气体不能燃烧也不助燃,所以如果生成物中的固体是碳酸钙,则实验现象是有气泡生成,燃着的木条熄灭;
②因为二氧化碳气体可与氢氧化钙反应,生成碳酸钙白色沉淀,所以如果生成物中的气体是二氧化碳,则将生成气体通入石灰水中,实验现象是石灰水变浑浊.
碳酸钙与盐酸反应化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,
Ca(HCO3)2受热分解的化学方程式为:Ca(HCO3)2
CaCO3↓+H2O+CO2↑.
故答案为:二氧化碳
CaCO3+2HCl═CaCl2+H2O+CO2↑,
Ca(HCO3)2
CaCO3↓+H2O+CO2↑.
②因为二氧化碳气体可与氢氧化钙反应,生成碳酸钙白色沉淀,所以如果生成物中的气体是二氧化碳,则将生成气体通入石灰水中,实验现象是石灰水变浑浊.
碳酸钙与盐酸反应化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,
Ca(HCO3)2受热分解的化学方程式为:Ca(HCO3)2
| ||
故答案为:二氧化碳
| 实验步骤 | 猜想正确应该的实验现象 |
| 有气泡生成;木条火焰熄灭 | |
| 石灰水 | 石灰水变浑浊 |
Ca(HCO3)2
| ||
点评:此题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
(4分)家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢(如图)。原因是硬水中含有较多的可溶性的钙和镁的化合物,其中碳酸氢钙[Ca(HCO3)2] 受热易分解,生成水和大量的气体,还生成一种难溶于水的化合物,它是水垢的主要成分。
[产生问题] 碳酸氢钙受热分解除了生成水以外,另外两种生成物是什么?
[提出假设] ① 小楠同学认为生成难溶于水的化合物可能是碳酸钙。
② 小卓同学根据 定律猜想生成物的气体可能是二氧化碳。
[实验与事实] 依据猜想他们设计了如下实验方案:
|
|
实验步骤 |
实验现象 |
|
验证猜想的①方案 |
向生成的难溶于水的化合物中加入适量的 。 |
有气泡生成 |
|
验证猜想②的方案 |
取少量硬水于试管并加热,将生成气 体通入 中。 |
可观察到 。 |
[解释与结论]:水垢主要成分之一是碳酸钙。
 36、同学们你们是否注意过家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢(如图).原因是硬水中含有较多的可溶性的钙和镁的化合物,其中碳酸氢钙[Ca(HCO3)2]受热易分解,生成水和大量的气体,还生成一种难溶于水的化合物,它是水垢的主要成分.
36、同学们你们是否注意过家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢(如图).原因是硬水中含有较多的可溶性的钙和镁的化合物,其中碳酸氢钙[Ca(HCO3)2]受热易分解,生成水和大量的气体,还生成一种难溶于水的化合物,它是水垢的主要成分.
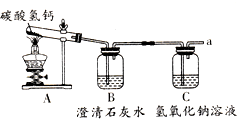 探究小组同学发现家中烧开水的铝壶和盛放开水的暖瓶,长时间使用会有白色固体附着,很难洗掉.
探究小组同学发现家中烧开水的铝壶和盛放开水的暖瓶,长时间使用会有白色固体附着,很难洗掉.