题目内容
取25克含有杂质的碳酸钙样品,跟盐酸反应(所含杂质不跟盐酸反应).反应完全时,共用去质量分数为10%的盐酸14.6克,计算该样品中碳酸钙的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据大理石的主要成分碳酸钙与盐酸反应的化学方程式,由参加反应盐酸的质量计算出大理石中碳酸钙的质量,而求得该大理石中碳酸钙的质量分数;
解答:解:设25g大理石中碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
x 14.6g×10%
=
x=20g
大理石中碳酸钙的质量分数=
×100%=80%
答案:大理石中碳酸钙的质量分数为80%.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
x 14.6g×10%
| 100 |
| 73 |
| x |
| 14.6g×10% |
x=20g
大理石中碳酸钙的质量分数=
| 20g |
| 25g |
答案:大理石中碳酸钙的质量分数为80%.
点评:解答本题时需要注意:14.6g为稀盐酸的溶液质量,而根据化学方程式的计算所使用的必须为纯净物的质量,因此不能直接使用溶液质量进行计算.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
A、B、C三种物质各15g,它们化合时只能生成30g新物质D.若增加10gA,则反应停止后,原反应物中只余C.根据上述条件推断下列说法中错误的是( )
| A、第一次反应停止后,B剩余6g |
| B、第二次反应后,D的质量为50g |
| C、反应中A和B的质量比是5:2 |
| D、反应中A和C的质量比是5:2 |
下列各组物质中,前者是化合物,后者是混合物的是( )
| A、冰水混合物 洁净的空气 |
| B、液氧 氯酸钾 |
| C、高锰酸钾分解后的固体剩余物 双氧水 |
| D、红磷 矿泉水 |
 (1)现在使用的氮肥大多是尿素[CO(NH2)2]和碳酸氢铵[NH4HCO3],请计算两种氮肥的相对分子质量.
(1)现在使用的氮肥大多是尿素[CO(NH2)2]和碳酸氢铵[NH4HCO3],请计算两种氮肥的相对分子质量.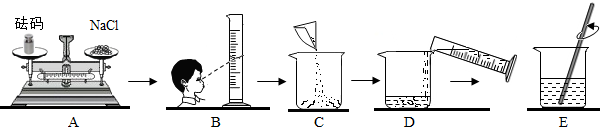
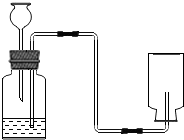 如图是实验室制取CO2装置图.
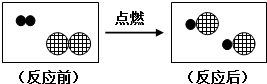
如图是实验室制取CO2装置图. ”表示H原子,用“
”表示H原子,用“ ”表示Cl原子,则下图中反应后容器内的物质属于
”表示Cl原子,则下图中反应后容器内的物质属于