题目内容
【题目】矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水PH和重金属含量达到排放标准。
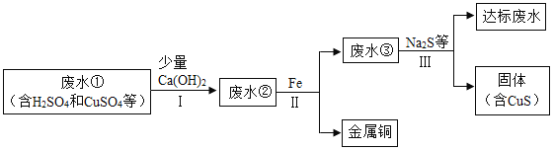
已知:步骤I无蓝色沉淀生成。
(1)步骤Ⅱ和步骤III都需进行的操作是_____,该操作中玻璃棒作用是_____。
(2)步骤Ⅱ得到金属铜的反应的化学方程式为_____。
(3)加入Ca(OH)2可以降低铁屑的消耗量,原因是_____。
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因是其中_____。
【答案】过滤 引流作用 Fe+ CuSO4 =Cu + FeSO4 氢氧化钙可以中和原溶液中的稀硫酸 含有CuSO4(或Cu2+)
【解析】
(1)步骤Ⅱ和步骤III都是将固体和液体分离,故是过滤,该操作中玻璃棒起引流作用。
(2)该步骤中铁与硫酸铜反应生成铜和硫酸亚铁,反应的方程式为:Fe+ CuSO4 =Cu + FeSO4。
(3)氢氧化钙可以中和原溶液中的稀硫酸,故可以减少铁的消耗。
(4)由于步骤Ⅲ加入Na2S后产生CuS,说明原废水③中含有CuSO4(或Cu2+)。

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目