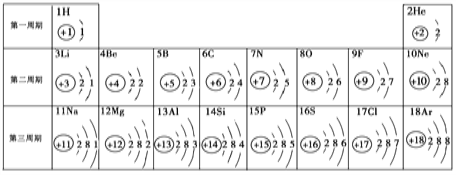
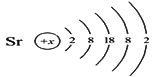
题目内容
【题目】为了验证某混合气体是由水蒸气、一氧化碳、二氧化碳三种气体组成,设计了如下实验方案:
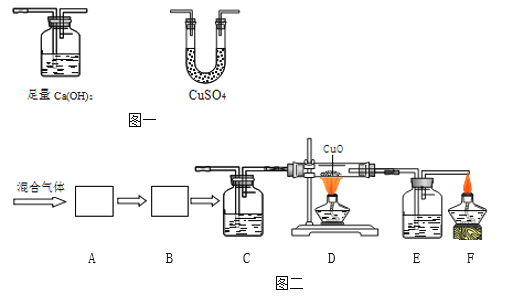
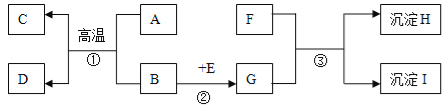
(1)验证混合气体中含有二氧化碳和水蒸气,在图二的A、B处依次放置________(填图一中的编号);请写出检验水蒸气的化学方程式:__________________。
(2)在图二中装置C、E的作用分别是___________________、__________________。
若没有装置C或E_____(填“能”或“否”)证明混合气体中含有一氧化碳,请简述原因_______________________。
【答案】Ⅱ ⅠH2O+5CuSO4 →CuSO4·5H2OC中澄清石灰水为了证明混合气体中二氧化碳是否被除尽E中澄清石灰水为了证明生成物中是否含有二氧化碳能观察到D中黑色固体变红色和尾气能点燃即可证明混合气体中含有一氧化碳
【解析】(1). 验证混合气体中含有二氧化碳和水蒸气时,为保证结果的准确性,要先用无水硫酸铜变蓝验证水,然后再通过澄清的石灰水变浑浊验证二氧化碳, (2). 硫酸铜和水反应的方程式为:H2O+5CuSO4 →CuSO4·5H2O (3). C中澄清石灰水变浑浊证明混合气体中二氧化碳被除尽,反之,没有除尽 (4). E中澄清石灰水则证明生成物中含有二氧化碳 ,反之,没有二氧化碳 (5). 若没有装置C或E也能证明混合气体中含有一氧化碳 (6).因为混合气体中只有一氧化碳有还原性,能将氧化铜还原成单质铜, 混合气体中只有一氧化碳有可燃性,所以观察到D中黑色固体变红色,和尾气能点燃即可证明混合气体中含有一氧化碳

【题目】实验室常用下列装置来制取气体,并完成相关性质实验探究。回答有关问题:
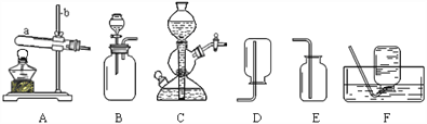
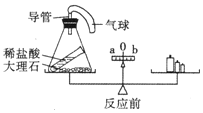
① 仪器a、b的名称是____________、 __________。
② 实验室用氯酸钾和二氧化锰混合共热制取一瓶干燥的氧气,需要选择的装置组合
是_________,化学方程式是____________。
③ 实验室用块状大理石和稀盐酸反应制取二氧化碳气体,选择的发生装置是C,该发生装置的名称叫___________,优点是__________,图示为反应的_____(填“进行”或“停止”)状态;充分反应后,向反应后的混合溶液中加入锌粒,产生气泡,则混合溶液中的溶质成分为________(填写化学式)。
④ 同学们在进行实验探究时发现很多因素都会对实验结果产生影响。
实验 | 分析与结论 |
Ⅰ.硫在空气中燃烧发出微弱的淡蓝色火焰, 硫在氧气中燃烧发出______________。 | 说明反应物的浓度不同,反应现象不同。 |
Ⅱ.细铁丝在氧气中易燃烧,化学方程式是________, 粗铁丝在氧气中不易燃烧。 | 说明_____________, 反应的速率不同。 |
Ⅲ.碳在氧气不足的条件下燃烧生成一氧化碳, 碳在氧气充足的条件下燃烧生成二氧化碳。 | 说明反应物的用量不同,________。 |
【题目】如表是硝酸钾、氯化钠在不同温度下的溶解度.
温度/℃ | 10 | 20 | 30 | 40 | 50 |
硝酸钾的溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
氯化钠的溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)从表中数据分析,溶解度受温度影响较大的物质是__________,硝酸钾和氯化钠溶解度曲线的交点在__________(填字母序号)之间.
A.20℃~30℃ B.30℃~40℃ C.40℃~50℃
(2)20℃,将50g硝酸钾与100g水混合,充分搅拌后静置,得到的溶液的质量是_________,是硝酸钾的__________(“饱和”或“不饱和”)溶液,若将温度升高到40℃,该溶解溶质的质量分数为__________(精确到0.1%).
(3)保持温度为20℃,将氯化钠的不饱和溶液变成饱和溶液,写出一种可行的方法__________。