题目内容
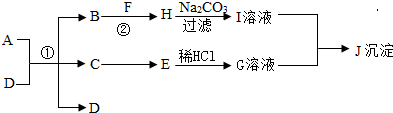
27、下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,下图是它们之间的转化关系,请回答:

(1)写出下列物质的化学式:F
(2)得到溶液I的操作名称为
(3)若G为无色溶液,J为白色沉淀,则E的化学式可能为
(4)若J为蓝色沉淀,写出I+G→J的化学方程式
(5)若反应前后元素的化合价发生改变,则属于氧化还原反应,请判断反应①、②、③中属于氧化还原反应的是

(1)写出下列物质的化学式:F
CaO
,C
O2
(2)得到溶液I的操作名称为
过滤
(3)若G为无色溶液,J为白色沉淀,则E的化学式可能为
MgO
(4)若J为蓝色沉淀,写出I+G→J的化学方程式
2NaOH+CuCl2=Cu(OH)2↓+2NaCl
(5)若反应前后元素的化合价发生改变,则属于氧化还原反应,请判断反应①、②、③中属于氧化还原反应的是
①
分析:H为改良酸性土壤常用的物质,可确定物质H为氢氧化钙;而反应①中物质D变化前后未变,为该反应的催化剂,反应中有催化剂的为过氧化氢的分解,因此A为过氧化氢,而B、C为水或氧气;物质B可与氧化物F反应生成氢氧化钙,则可判断B为水,则C为氧气;至此,本题的推断找到的突破口,并展开了对物质间反应关系的逐步推断;据此,完成本题的判断.
解答:解:(1)H为改良酸性土壤常用的物质,则H为氢氧化钙;B为水,水与氧化钙反应生成氢氧化钙,则B为氧化钙;过氧化氢A分解生成B水和氧气,所以C为氧气;
故答案为:CaO;O2;
(2)氢氧化钙与碳酸钠反应生成氢氧化钠溶液和碳酸钙沉淀,通过过滤把沉淀与溶液分离开来;
故答案为:过滤;
(3)能与稀盐酸反应的氧化物E一定是金属氧化物,则反应生成的G应为可溶性氯化物的溶液,再与氢氧化钠溶液进行反应,生成氯化钠与另一种不溶性的碱J;且J为白色沉淀,如氢氧化镁、氢氧化铝、氢氧化锌等白色沉淀,则G为氯化镁或氯化铝、氯化锌等;则E物质就可能是氧化镁、氧化铝或氧化锌等氧化物;
故答案为:MgO(ZnO等合理即可);
(4)J为蓝色沉淀即氢氧化铜沉淀,则G为氯化铜溶液,氯化铜与氢氧化钠生成蓝色氢氧化铜沉淀和氯化钠溶液;
故答案为:2NaOH+CuCl2=Cu(OH)2↓+2NaCl;
(5)反应①,过氧化氢分解生成水和氧气,过氧化氢中氧为-1价而水中氧为-2价、氧气中O为价,反应前后有化合合的变化,为氧化还原反应;反应②为氧化钙与水化合成氢氧化钙,反应前后无化合价改变,不属于氧化还原反应;反应③金属氧化物与盐酸发生的复分解反应,复分解反应前后元素化合价都不改变,不属于氧化还原反应;
故答案为:①.
故答案为:CaO;O2;
(2)氢氧化钙与碳酸钠反应生成氢氧化钠溶液和碳酸钙沉淀,通过过滤把沉淀与溶液分离开来;
故答案为:过滤;
(3)能与稀盐酸反应的氧化物E一定是金属氧化物,则反应生成的G应为可溶性氯化物的溶液,再与氢氧化钠溶液进行反应,生成氯化钠与另一种不溶性的碱J;且J为白色沉淀,如氢氧化镁、氢氧化铝、氢氧化锌等白色沉淀,则G为氯化镁或氯化铝、氯化锌等;则E物质就可能是氧化镁、氧化铝或氧化锌等氧化物;
故答案为:MgO(ZnO等合理即可);
(4)J为蓝色沉淀即氢氧化铜沉淀,则G为氯化铜溶液,氯化铜与氢氧化钠生成蓝色氢氧化铜沉淀和氯化钠溶液;
故答案为:2NaOH+CuCl2=Cu(OH)2↓+2NaCl;
(5)反应①,过氧化氢分解生成水和氧气,过氧化氢中氧为-1价而水中氧为-2价、氧气中O为价,反应前后有化合合的变化,为氧化还原反应;反应②为氧化钙与水化合成氢氧化钙,反应前后无化合价改变,不属于氧化还原反应;反应③金属氧化物与盐酸发生的复分解反应,复分解反应前后元素化合价都不改变,不属于氧化还原反应;
故答案为:①.
点评:反应中化合价的变化规律:有单质参加的反应,反应前后一定出现元素的化合价的改变;而复分解反应是反应前后元素化合价一定不发生改变的基本反应类型.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目