题目内容
【题目】” 毒淀粉”是在淀粉中添加了对人体有害的马来酸( C4H4O4 ),下列说法正确的是
A.马来酸中各元素的质量比是48 : 4 : 64
B.马来酸中含有3个元素
C.马来酸中含有4个碳原子、4个氢原子和4个氧原子
D.马来酸和青蒿素( C15H23O5 )分别在氧气中完全燃烧的产物相同
【答案】D
【解析】
元素的质量比等于元素的相对原子质量乘以原子个数的比。
A、马来酸化学式为C4H4O4,碳、氢、氧三种元素的质量比为![]() ,故A不正确;
,故A不正确;
B、马来酸化学式为C4H4O4,含有碳、氢、氧三种元素,故B不正确;
C、马来酸是由分子构成的,1个马来酸分子中含有4个碳原子、4个氢原子和4个氧原子,故C不正确;
D、马来酸和青蒿素都是由碳、氢、氧三种元素组成的,在氧气中完全燃烧的产物均为二氧化碳和水,故D正确。故选D。

【题目】为测定石灰石样品的纯度,取4g该样品,将40g稀盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据见下表。
次数 | 1 | 2 | 3 | 4 |
加入盐酸质量/g | 10 | 10 | 10 | 10 |
剩余固体质量/g | 2.5 | 1.0 | 0.4 | 0.4 |
(1)该石灰石样品中碳酸钙的质量分数是_____;
(2)求100g这种石灰石跟足量盐酸反应,生成二氧化碳的质量_____。
【题目】竹子是“有节、中空、四季常绿”的植物。同学们对竹子中的气体成分展开了探究,测定其成分
[提出猜想]猜想一:气体成分含有_____,猜想二:气体成分含有_____,
(1)收集竹子中的气体。
小华提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体。
小刚提出:可用注射器从竹子中抽取气体。
大家认为两人的想法都可行,于是分为A、B两组,在相同条件下,A组采用小华的取气方法,B组采用小刚的取气方法,分别完成下面的实验。
(2)检验气体中是否含有二氧化碳气体。
实验步骤 | 实验现象 | 实验结论及解释 |
向所取得气体中加入_____。 | _____ 。 | 有二氧化碳 |
(3)测定氧气含量。
[查阅资料]红磷的着火点为240°C,白磷的着火点为40°C。
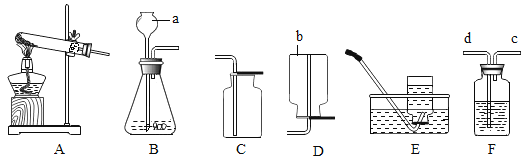
[设计实验]同学们设计了如图所示的方案一和方案二来测定氧气含量。
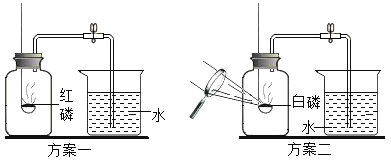
[进行实验]按上述两个方案进行多次实验。
[反思与评价]
a.实验中磷的量应为足量,原因是_____,
b.两个方案的实验测定结果不同,大家经讨论后一直认为方案_____(选填“一“或“二”)测定结果比较准确。原因是_____。
c.经过A. B两组同学将收到的气体尽管都用比较准确的方案实验,但A的误差较大,导致这种结果的原因可能是_____。