题目内容
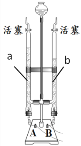
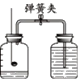
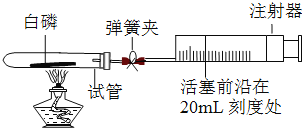
【题目】为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器.将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.假设此实验能按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
(1)实验前,打开弹簧夹,将注射器的活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明________;
(2)若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等到试管冷却后再松开弹簧夹.可观察到的现象为______;
(3)若不使用弹簧夹,用酒精灯加热白磷,充分反应直至燃烧结束,试管冷却.可观察到的现象为______;
(4)试管中发生的反应的文字表达式:______.
【答案】装置的气密性好; 白磷燃烧,产生白烟,活塞前沿约在12mL的刻度线上; 白磷燃烧,产生白烟,活塞先向右移动,最终稳定在约8mL的刻度线上; 磷+氧气![]() 五氧化二磷;
五氧化二磷;
【解析】
(1)打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明整个装置都不漏气;
(2)若先夹紧弹簧夹,用酒精灯加热白磷,这时白磷燃烧消耗掉的只是试管内的氧气为40mL×![]() =8mL,所以活塞应停在20mL﹣8mL=12mL的刻度处;
=8mL,所以活塞应停在20mL﹣8mL=12mL的刻度处;
(3)白磷燃烧放出热量,容器内的气压先增大,冷却后气压降低。若不使用弹簧夹,用酒精灯加热白磷,白磷实际消耗掉的是试管40mL和注射器内20mL的氧气为(40mL+20mL)×![]() =12mL,活塞应停在20mL﹣12mL=8mL的刻度处。因此可观察到的现象为白磷燃烧,产生白烟,活塞先向右移动,最终稳定在约8mL的刻度线上;
=12mL,活塞应停在20mL﹣12mL=8mL的刻度处。因此可观察到的现象为白磷燃烧,产生白烟,活塞先向右移动,最终稳定在约8mL的刻度线上;
(4)白磷的燃烧是磷与氧气发生反应生成了五氧化二磷,反应的文字表达式为:磷+氧气![]() 五氧化二磷。
五氧化二磷。

 名校课堂系列答案
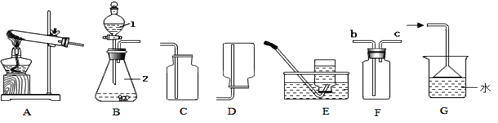
名校课堂系列答案【题目】下列实验设计不能达到实验目的是( )
选项 | A | B | C | D |
实验设计 |
|
|
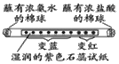
| 信息:氨水能使湿润 紫色石蕊试纸变蓝; 盐酸能使湿润紫色 石蕊试纸变红
|
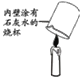
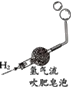
实验 目的 | 红磷燃烧测定空气中氧气的含量 | 探究石蜡燃烧后有二氧化碳生成 | 验证氢气的密度比空气小 | 不同分子运动速率 |
A. A B. B C. C D. D