题目内容
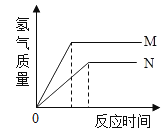
【题目】相同质量的M、N两种金属,分别与相同质量分数且足量的稀盐酸反应生成+2价的盐,生成氢气质量和反应时间的关系如图所示。说法正确的是( )
A.金属的活动性:M<N
B.相对原子质量:M<N
C.消耗盐酸质量:M=N
D.生成氢气质量:M=N
【答案】B
【解析】
A、根据反应生成氢气的质量与反应时间的关系图所示,相同时间内M放出氢气的质量大于N,可判断金属活动性顺序是M>N,故说法错误;
B、M、N金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成氢气的质量与反应时间的关系图所示,在金属完全反应后,放出氢气的质量是M>N,因此可判断相对原子质量是N>M,故说法正确;
C、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗稀盐酸的质量:M>N,故说法错误;
D、根据反应生成氢气的质量与反应时间的关系图所示,在两种金属完全反应后,放出氢气的质量是M>N,故说法错误;
故选:B。

【题目】实验课上,李杰拿出一片黄色的金属向同学炫耀说他捡到了黄金,张峰说他曾在网上看到过,有一种铜锌合金外观和黄金相似,常被误认为是黄金。于是他与李杰开始探究。
(提出问题)这块黄色金属是黄金?还是铜锌合金?
(猜 想)①李杰认为是黄金 ②张峰认为是铜锌合金
(查阅资料)合金中的金属保持各自的化学性质,金在高温下不与氧气反应,锌在高温下与氧气反应生成白色固体。
(设计实验)李杰设计的实验是:截取一小片黄色的金属放在石棉网上用酒精灯加热;张峰设计的实验是:截取一小片黄色的金属放入硝酸银溶液中。
(现象与结论)李杰在实验中观察到黄色的金属变黑,则他的猜想_____(填“正确”或“错误”),黑色物质是_____。张峰在实验中观察到的现象是_____,反应的化学方程式为_____(只写一个)。
(反思与应用)假如你与张峰的观点相同,请你设计另一实验方案并完成下列实验报告。
实验操作 | 实验现象 | 化学方程式 |
截取一小片黄色金属放入_____溶液中. | _____ | _____ |
【题目】下列叙述I和II都正确且有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 碳具有还原性 | 焦炭可以还原四氧化三铁 |
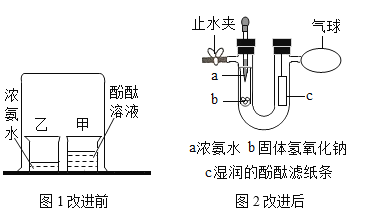
B | 分子之间有间隔 | 浓氨水和浓盐酸接近时“空中生烟” |
C | 人体碘元素摄入量不足 | 易患有骨质疏松症 |
D | 二氧化碳支持燃烧 | 二氧化碳能使澄清石灰水变浑浊 |
A.AB.BC.CD.D