题目内容
从某碳酸盐矿石(主要成分是BaCO3和CaCO3)中提炼BaCO3(尽可能除去Ca2+).现查得一些溶解度(g/100g水)数据.原料只有该矿石、水、燃料,要求Ca2+ 含量越低越好.
| 0℃ | 50℃ | 80℃ | |
| Ca(OH)2 | 0.173 | 0.130 | 0.094 |
| Ba(OH)2 | 1.64 | 13.1 | 101.5 |

(2)写出下列反应的化学方程式:
A→B______;
B→C______;
D→E______.
解:(1)根据课本所学信息可知:①矿石高温煅烧可得氧化物;②氧化物与水生成氢氧化物;③氢氧化钙的溶解度随温度升高而减少,而氢氧化钡的溶解度随温度的升高而增大,所以分离它们,可加热过滤;④氢氧化钙被过滤出来,知识迁移,氢氧化钡也和二氧化碳反应,用生成的二氧化碳与氢氧化钡反应生成碳酸钡.
(2)根据(1)中化学反应流程图书写化学方程式.
故答案为:
(1)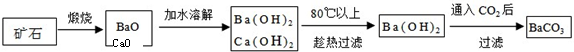
(2)由A→B:CaCO3 CaO+CO2↑ BaCO3
CaO+CO2↑ BaCO3 BaO+CO2↑;
BaO+CO2↑;
由B→C:CaO+H2O═Ca(OH)2;BaO+H2O═Ba(OH)2;
由D→E:Ba(OH)2+CO2═BaCO3↓+H2O
分析:(1)根据BaCO3和CaCO3高温煅烧都可以分解成为氧化物,金属氧化物会与水生成碱,氢氧化钙和氢氧化钡溶解度的区别进行分析;
(2)根据(1)中的流程图书写化学方程式;
点评:在解此类题时,首先分析题中的反应原理,了解碳酸钡与碳酸钙的性质,然后结合题中的信息和最后得到的物质进行分析.
(2)根据(1)中化学反应流程图书写化学方程式.
故答案为:
(1)
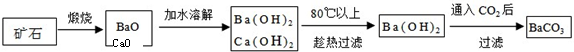
(2)由A→B:CaCO3
 CaO+CO2↑ BaCO3
CaO+CO2↑ BaCO3 BaO+CO2↑;
BaO+CO2↑;由B→C:CaO+H2O═Ca(OH)2;BaO+H2O═Ba(OH)2;
由D→E:Ba(OH)2+CO2═BaCO3↓+H2O
分析:(1)根据BaCO3和CaCO3高温煅烧都可以分解成为氧化物,金属氧化物会与水生成碱,氢氧化钙和氢氧化钡溶解度的区别进行分析;
(2)根据(1)中的流程图书写化学方程式;
点评:在解此类题时,首先分析题中的反应原理,了解碳酸钡与碳酸钙的性质,然后结合题中的信息和最后得到的物质进行分析.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
从某碳酸盐矿石(主要成分是BaCO3和CaCO3)中提炼BaCO3(尽可能除去Ca2+).现查得一些溶解度(g/100g水)数据.原料只有该矿石、水、燃料,要求Ca2+ 含量越低越好.
(1)下图为分离步骤,把反应条件、方法或所需物质写在箭头上(或下)方,方框内写出每步产物的化学式
(2)写出下列反应的化学方程式:
A→B______ CaO+CO2↑ BaCO3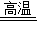 BaO+CO2↑;
BaO+CO2↑;
| 0℃ | 50℃ | 80℃ | |
| Ca(OH)2 | 0.173 | 0.130 | 0.094 |
| Ba(OH)2 | 1.64 | 13.1 | 101.5 |

(2)写出下列反应的化学方程式:
A→B______ CaO+CO2↑ BaCO3
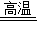 BaO+CO2↑;
BaO+CO2↑;
从某碳酸盐矿石(主要成分是BaCO3和CaCO3)中提炼BaCO3(尽可能除去Ca2+).现查得一些溶解度(g/100g水)数据.原料只有该矿石、水、燃料,要求Ca2+ 含量越低越好.
(1)下图为分离步骤,把反应条件、方法或所需物质写在箭头上(或下)方,方框内写出每步产物的化学式
(2)写出下列反应的化学方程式:
A→B______ CaO+CO2↑ BaCO3 BaO+CO2↑;
BaO+CO2↑;
| 0℃ | 50℃ | 80℃ | |
| Ca(OH)2 | 0.173 | 0.130 | 0.094 |
| Ba(OH)2 | 1.64 | 13.1 | 101.5 |

(2)写出下列反应的化学方程式:
A→B______ CaO+CO2↑ BaCO3
 BaO+CO2↑;
BaO+CO2↑; 
