题目内容
根据KNO3和NaCl的溶解度曲线,回答问题:
(1)30℃时KNO3的溶解度
(2)若将t℃的两者等质量的饱和溶液同时降温至0℃,晶体析出较多的是
(3)工业上采用如下的流程从海水中提取精盐:工业上采用如下的流程从海水中提取精盐:
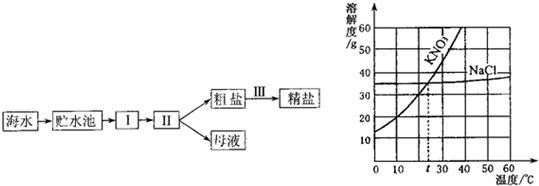
上述流程中Ⅰ为
(4)现要配制500千克16%的氯化钠溶液来选种,需要20%的氯化钠溶液
(1)30℃时KNO3的溶解度
>
>
(填“>”、“<”或“=”)NaCl的溶解度.(2)若将t℃的两者等质量的饱和溶液同时降温至0℃,晶体析出较多的是
硝酸钾
硝酸钾
.(3)工业上采用如下的流程从海水中提取精盐:工业上采用如下的流程从海水中提取精盐:

上述流程中Ⅰ为
蒸发
蒸发
、母液是氯化钠的饱和
饱和
溶液(填“饱和”、“不饱和”).若在实验室中完成上述流程中Ⅲ,需经过溶解、过滤
过滤
、蒸发
蒸发
三步完成,这三步都要用到的玻璃仪器是玻璃棒
玻璃棒
.(4)现要配制500千克16%的氯化钠溶液来选种,需要20%的氯化钠溶液
400
400
千克.分析:(1)根据题中硝酸钾和氯化钠溶解度曲线分析.
(2)根据硝酸钾和氯化钠的溶解度都随温度升高而增大但硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小分析.
(3)根据从海水中提取精盐要经过日晒蒸发水分然后过滤得到粗盐,再将粗盐溶解过滤蒸发即可得到精盐;在溶解、过滤、蒸发中都用到玻璃仪器玻璃棒分析.
(4)根据溶质质量分数=
×100%的变形公式计算.
(2)根据硝酸钾和氯化钠的溶解度都随温度升高而增大但硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小分析.
(3)根据从海水中提取精盐要经过日晒蒸发水分然后过滤得到粗盐,再将粗盐溶解过滤蒸发即可得到精盐;在溶解、过滤、蒸发中都用到玻璃仪器玻璃棒分析.
(4)根据溶质质量分数=
| 溶质质量 |
| 溶液质量 |
解答:解:(1)从硝酸钾和氯化钠溶解度曲线可以看出30℃时KNO3的溶解度大于氯化钠的溶解度,故答案:>.
(2)硝酸钾和氯化钠的溶解度都随温度升高而增大但硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小,所以t℃的两者等质量的饱和溶液同时降温至0℃,晶体析出较多的是硝酸钾,故答案:硝酸钾.
(3)从海水中提取精盐要经过日晒蒸发水分,然后过滤得到粗盐,得到的母液不能再溶解食盐所以是食盐的饱和溶液;再将粗盐溶解过滤蒸发即可得到精盐;在溶解、过滤、蒸发中都用到玻璃仪器玻璃棒,故答案:蒸发;饱和;过滤;蒸发.
(4)配制500千克16%的氯化钠溶液,其中溶质氯化钠的质量为500kg×16%=80kg,需要20%的氯化钠溶液的质量为:
=400kg,故答案:400kg.
(2)硝酸钾和氯化钠的溶解度都随温度升高而增大但硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小,所以t℃的两者等质量的饱和溶液同时降温至0℃,晶体析出较多的是硝酸钾,故答案:硝酸钾.
(3)从海水中提取精盐要经过日晒蒸发水分,然后过滤得到粗盐,得到的母液不能再溶解食盐所以是食盐的饱和溶液;再将粗盐溶解过滤蒸发即可得到精盐;在溶解、过滤、蒸发中都用到玻璃仪器玻璃棒,故答案:蒸发;饱和;过滤;蒸发.
(4)配制500千克16%的氯化钠溶液,其中溶质氯化钠的质量为500kg×16%=80kg,需要20%的氯化钠溶液的质量为:
| 80kg |
| 20% |
点评:粗盐提纯的步骤包括:溶解、过滤、蒸发.在这三步中都用到玻璃棒,溶解时玻璃棒搅拌能加快溶解;过滤时玻璃棒引流液体;蒸发用玻璃棒搅拌即能加快蒸发也能防止局部受热造成液滴飞溅.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
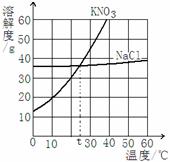 24、(1)现有60℃的饱和NaCl溶液,与该溶液有关的量有:①水的质量;②溶液中溶质NaCl的质量;③NaCl的质量分数;④60℃时NaCl的溶解度:⑤溶液的质量.用序号填空:
24、(1)现有60℃的饱和NaCl溶液,与该溶液有关的量有:①水的质量;②溶液中溶质NaCl的质量;③NaCl的质量分数;④60℃时NaCl的溶解度:⑤溶液的质量.用序号填空: (2008?自贡)根据KNO3和NaCl的溶解度曲线,回答下列问题:
(2008?自贡)根据KNO3和NaCl的溶解度曲线,回答下列问题: 根据KNO3和NaCl的溶解度曲线,回答问题:
根据KNO3和NaCl的溶解度曲线,回答问题: 根据KNO3和NaCl的溶解度曲线,回答下列问题:
根据KNO3和NaCl的溶解度曲线,回答下列问题: