题目内容
【题目】实验室有一瓶溶质质量分数未知的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8g10%的氢氧化钠溶液,然后往烧杯中逐滴滴加该盐酸,反应过程中溶液的pH与滴入盐酸的质量关系如图所示,请回答下列问题: 
(1)配置了8g10%的氢氧化钠溶液,需要水的质量为;
(2)计算该盐酸的溶质质量分数:(写出计算过程)
【答案】
(1)7.2g
(2)解:设10g稀盐酸中氯化氢的质量为x,
NaOH+ | HCl═NaCl+H2O |
40 | 36.5 |
8g×10% | x |
![]() ,
,
x=0.73g,
该盐酸的溶质质量分数为: ![]() ×100%=7.3%,
×100%=7.3%,
答:该盐酸的溶质质量分数为7.3%.
【解析】解:(1)配制8g10%的NaOH溶液,需要水的质量为:8g×(1﹣10%)=7.2g; 故填:7.2g.
【考点精析】解答此题的关键在于理解根据化学反应方程式的计算的相关知识,掌握各物质间质量比=系数×相对分子质量之比.

练习册系列答案
相关题目
【题目】实验室部分装置如图所示,回答下列问题(制取时将A中的药品混合). 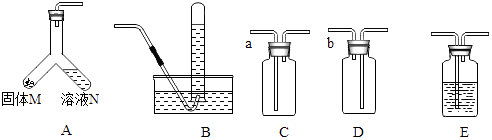
(1)已知图中a、b均为气体的入口,要制取并收集不同气体,请填写如表空白.
固体M | 溶液N | 制取的气体 | 收集装置(填字母) |
大理石 | 稀盐酸 | CO2 | |
锌粒 | 稀硫酸 | B或D | |
O2 | B或C |
(2)收集干燥的CO2还需要用装置E,E中盛装的试剂为 .
(3)制取少量气体时,用上述装置A的优点是(写一点即可).